Длительный гидролиз
Cтраница 1
Длительный гидролиз ( 72 часа) требуется для расщепления связи между валином и изолей-цином, которая чрезвычайно устойчива к кислоте. [1]
Длительный гидролиз в условиях обычной лабораторной атмосферы может приводить к образованию на поверхности так называемых фейткнехтовских фаз [97] основного азида свинца, которые могут реагировать с атмосферной двуокисью углерода. Хорошо состаренный а-азид определенно бывает покрыт основным карбонатом, который легко разлагается уже в начале опыта с выделением двуокиси углерода и азотистоводородной кислоты, что сильно осложняет последующий кинетический анализ основной реакции. В некоторой мере его значение было разъяснено в двух последних статьях Рейтцнера [101], в которых, однако, кинетика реакции не рассматривается. [2]
Более длительный гидролиз заметно понижает выход аргинина. Чем дольше проводится кипячение, тем больше повышается количество образующегося в гидролизате аммиака. Поэтому целесообразно проводить гидролиз нескольких порций белка в течение разного периода времени - от 5 до 24 час. Гидролизат разбавляют таким образом, чтобы в каждых 5 мл содержалось 20 - - 40 мг аргинина. [3]
Более длительный гидролиз в этих условиях приводит к заметным потерям адешша. [4]
При длительном гидролизе фермент к субстрату добавляют двумя или тремя порциями. Природа буфера, используемого для гидролиза, зависит от характера последующей работы. [5]
Эта методика исключает длительный гидролиз найлонов. [6]
Следует иметь в виду, что при таком длительном гидролизе происходит распад 10 % содержащейся в растворе фруктозы. [7]
В работе важно уловить нужный момент для йодной пробы, так как при длительном гидролизе полное расщепление крахмала может произойти и при более низкой температуре опыта. Результаты работы фиксируют в таблице. [8]
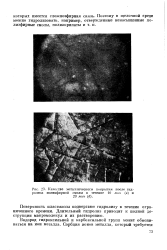 |
Качество металлического покрытия после гидролиза полиэфирной смолы в течение 10 мин ( а и 20 мин ( б. [9] |
Поверхность пластмассы подвергают гидролизу в течение ограниченного времени. Длительный гидролиз приводит к полной деструкции макромолекул и их растворению. [10]
Целлобиозу можно получить из целлюлозы, осторожно гидролизуя ее. Длительный гидролиз целлюлозы приводит к образованию глюкозы. Поскольку группы - ОН молекул глюкозы легко участвуют в конденсации, можно предположить, что глюкоза будет вступать и в; реакцию поликонденсации. Подобные полимеры глюкозы действительно существуют в природе в форме таких углеводов, как крахмал и целлюлоза. Гидролиз этих веществ приводит к их превращению в мономер глюкозы. [11]
Химотрипсии гораздо менее специфичен, чем трипсин. Избирательное расщепление пептидных связей, в которых принимают участие карбоксильные группы ароматических аминокислот, происходит только при краткосрочном гидролизе. Длительный гидролиз приводит к разрушению и других пептидных связей, например образованных остатками лейцина, гистидина и глутамина. [12]
Для гидролиза удобно пользоваться летучими буферными растворами ( после высушивания гидролизаты не содержат солей), например, раствором бикарбоната аммония. Время гидролиза ( от 2 до 12 ч) зависит от природы анализируемого белка. При длительном гидролизе во избежание автолиза фермент нередко добавляют к субстрату двумя или тремя порциями. [13]
Таким образом, в проведенной нами работе модифицирование электроповерхностных свойств происходило не вследствие изменения объемной фазы а благодаря изменению только свойств поверхностного слоя частиц Fe04 Наблюдаемое смещение точки нулевого заряда в область больших значений рН мо жет быть объяснено следующим образом. В случае правильности предлагаемого здесь объяснения точка нулевого заряда Fe2O3обработанного наиболее концентрированным раствором HUJ ( 11), должна приближаться к точке нулевого заряда образцов Fe20S) полученных длительным гидролизом солей железа. В связи с этим представляет интерес провести сравнение положений точек нулевого заряда с точками нулевого заряда, имеющимися в литературе. [15]
Страницы: 1 2