Окончательный гидролиз
Cтраница 2
В растворах пленкообразующих веществ должно осуществляться оптимальное соотношение исходного основного пленкообразующего вещества, растворителя и катализатора. Это должно одновременно обеспечить, с одной стороны, быстрый частичный или полный гидролиз в растворе с сохранением образующихся продуктов гидролиза соответствующих кислот или гидроокисей, элементов в виде золя и, с другой стороны, - мгновенный окончательный гидролиз в тонком слое на обрабатываемой поверхности с выделением прозрачной пленки соответствующей гидроокиси. Кроме того, только при оптимальных соотношениях компонентов в растворе образующиеся пленки сцепляются достаточно прочно с поверхностью обрабатываемого материала. [16]
Все эксперименты, описанные в настоящей главе, проводили з указанной области пересыщения. Стехиометрически ГФ, возможно, не осаждается при рН, температуре и содержании кальция и фосфата, встречаемых в большинстве природных систем. Окончательный гидролиз более кислых твердых фаз, осаждающихся первыми, до ГФ, возможно, занял бы значительные промежутки времени. ГФ становится термодинамически устойчивым в более щелочной среде до значения рН 13 - 14, при котором происходит осаждение гидроксида кальция. [17]
Скорость реверсии, как установлено Шенеманом, увеличивается не только благодаря воздействию кислоты, но и в особенности при повышении температуры. В результате этого при выпаривании соляной кислоты из гидролизата основной ступе - ни, в течение которого концентрация поднимается до 70 %, замечается весьма значительная реверсия вследствие смещения равновесия. Поэтому, указывает Шенеман, чтобы достичь высокого выхода кристаллической глюкозы, необходимо расщеплять молекулы дисахаридов ( как остаточные, так и вновь образующиеся) в процессе окончательного гидролиза - инверсии. Зависимость равновесия от концентрации требует, к сожалению, большого разбавления жидкости. Процессу сопутствуют вредные реакции, расщепляющие небольшое количество образованной глюкозы в гидроксиметилфурфурол и далее в леву-линовую и муравьиную кислоты. [18]
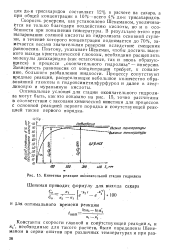 |
Кинетика реакции окончательной стадии гидролиза Шенеман приводит, формулу для выхода сахара. [19] |
Скорость реверсии, как установлено Шенеманом, увеличивается не только благодаря воздействию кислоты, но и в особенности при повышении температуры. В результате этого при выпаривании соляной кислоты из гидролизата основной ступе - ни, в течение которого концентрация поднимается до 70 %, замечается весьма значительная реверсия вследствие смещения равновесия. Поэтому, указывает Шенеман, чтобы достичь высокого выхода кристаллической глюкозы, необходимо расщеплять молекулы дисахаридов ( как остаточные, так и вновь образующиеся) в процессе окончательного гидролиза - инверсии. Зависимость равновесия от концентрации требует, к сожалению, большого разбавления жидкости. Процессу сопутствуют вредные реакции, расщепляющие небольшое количество образованной глюкозы в гидроксиметилфурфурол и далее в леву-линовую и муравьиную кислоты. [20]
Полученный таким образом ксантогенат растворяют в разбавленной щелочи; получается густая масса, называемая вискозой. Вискозу оставляют на некоторое время созревать; при этом происходит частичный гидролиз ксантоге-ната. После этого вискозу продавливают через платиновые колпачки с рядом мельчайших отверстий в разбавленную водой серную кислоту, к которой прибавлены еще некоторые соли. Здесь происходит окончательный гидролиз ксан-тогената. Сформированные таким образом ниточки клетчатки после промывки и отбелки высушивают. [21]
Полученный таким образом ксантогенат ра створяют в разбавленной щелочи; получается густая масса, называемая вискозой. Вискозу оставляют на некоторое время созревать; при этом происходит частичный гидролиз ксантоге-ната. После этого вискозу продавливают через платиновые колпачки с рядом мельчайших отверстий в разбавленную водой серную кислоту, к которой прибавлены еще некоторые соли. Здесь происходит окончательный гидролиз ксан-тогената. Сформированные таким образом ниточки клетчатки после промывки и отбелки высушивают. [22]
К ним относятся эстеразы. Эстеразы проводят гидролиз эфиров и жиров; карбогидразы расщепляют углеводы; протеазы, или протеолитпче-ские ферменты, расщепляют белковые вещества. Протеазы широко распространены в природе, и к ним относится большое число ферментов, не одинаковых по свойствам. Гидролиз белковых веществ протекает ступенчато с образованием промежуточных продуктов-аль-бумоз, пептонов, полипептидов и, наконец, х-аминокислот. Следующим ферментом является выделяемый поджелудочной железой трипсин, активно гидролизующий в щелочной среде ( рН - - 8 -: 9) и активируемый коферментом энтсрокинизои. Эта триптическая группа протеиназ расщепляет белки главным образом до полипептидов. Наконец, в кишечном соке имеется третья группа ферментов, называемая временном, которая завершает окончательный гидролиз полипептйдов до а-аминокислот. Исследования с изотопным азотом [82] показали, что в клетках животных организмов белки постоянно распадаются и снова синтезируются из а-аминокислот, причем и распад и синтез совершаются при участии одних и тех же ферментов. [23]
Ферменты, проводящие гидролиз, носят общее название гидролазы. Эстеразы проводят гидролиз эфиров и жиров; карбогидразы расщепляют углеводы; протеазы, или протеолитнче-ские ферменты, расщепляют белковые вещества. Протеазы широко распространены в природе, и к ним относится большое число ферментов, не одинаковых по свойствам. Гидролиз белковых веществ протекает ступенчато с образованием промежуточных продуктов-аль-бумоз, пептонов, полипептидов и, наконец, а-аминокислот. К ферментам, гидролизующим белковые вещества, в первую очередь относится пепсин-фермент желудочного сока, активный только в сильно кислой среде ( рН 1 5 - 2 5) и расщепляющий белки до альбумоз и пептонов. Следующим ферментом является выделяемый поджелудочной железой трипсин, активно гидролизующий в щелочной среде ( рН 8 - - 9) и активируемый коферментом энтсроциназой. Эта триптическая группа протеиназ расщепляет белки главным образом до полипептидов. Наконец, в кишечном соке имеется третья группа ферментов, называемая эрепсином, которая завершает окончательный гидролиз полипептидов до а-аминокислот. Исследования с изотопным азотом [32] показали, что в клетках животных организмов белки постоянно распадаются и снова синтезируются из а-аминокислот, причем и распад и синтез совершаются при участии одних и тех же ферментов. [24]
Страницы: 1 2