Гидроокись
Cтраница 2
Гидроокиси, образуемые этими катионами, являются слабыми основаниями и соли их сильно гидролизуются. Растворы таких солей имеют кислую реакцию и поэтому их нейтрализуют перед осаждением катионов. Соли, образованные некоторыми катионами и слабыми кислотами ( например, H2S, H2CO3 и др.), гидролизуются в такой степени, что практически в водных растворах не существуют. [16]
Гидроокиси и оксигидроокиси большинства описанных здесь металлов существуют в виде нескольких модификаций. [17]
Гидроокиси всех катионов третьей группы растворимы в кислотах. [18]
Гидроокиси каких катионов третьей группы обладают амфотерным характером. [19]
Гидроокиси всех катионов третьей группы растворимы в кислотах. [20]
Гидроокиси каких катионов третьей группы обладают амфотерным характером. [21]
Гидроокись или карбонат лития могут быть определены общепринятыми методами ацидометрии. Хлорид лития может быть оттитрован аргентометри-чески. [22]
Гидроокись ведет себя здесь как основание, так как избыток водородных ионов подавляет ионизацию по кислотному типу. Коллоидная частица при этом будет заряжена положительно. [23]
Гидроокиси получают в виде плотных хлопьевидных осадков, нерастворимых в избытке осадителя, действием едких щелочей на растворы солей редкоземельных элементов. Гидроокись трехвалентного церия является сильным восстановителем; на воздухе медленно принимает фиолетовую окраску и. Последняя растворяется в азотной кислоте с образованием окрашенного в оранжевый цвет раствора; с соляной кислотой образуется хлорид трехвалентного церия с выделением свободного хлора. [24]
Гидроокись осаждается из циркониевых растворов аммиаком или едкой щелочью. Белое желатинообразное вещество, нерастворимое в избытке осадителя, содержит неопределенное количество воды. Осажденная на холоду растворяется в разбавленных кислотах; но после осаждения из горячих растворов или после соприкосновения с горячей водой растворяется только в концентрированных кислотах. [25]
Гидроокиси сульфония являются сильными основаниями, полностью диссоциированными на ионы, подобными гидроокисям щелочных металлов. [26]
Гидроокиси Э ( ОН) 4 имеют амфотерный характер. [27]
Гидроокись осаждают из раствора прибавлением рассчитанного количества азотной кислоты, промывают до удаления анионов NOs и прессуют в таблетки. Такие катализаторы ( применяемые для лабораторных работ) содержат до 25 % окиси хрома. [28]
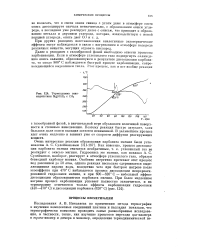 |
Термограмма взаимодействия Mg ( OH a с СОа. [29] |
Гидроокись же магния, как показал А. С. Сулейманов, наоборот, реагирует в атмосфере углекислого газа, образуя безводный карбонат магния. Особенно энергично протекает этот процесс под давлением до 50 апгм, однако реакция несколько сдерживается выделяющимися парами воды, вследствие чего при быстром нагреве после экзоэффекта при 470 С наблюдается процесс диссоциации непрореагировавшей гидроокиси магния, и при 600 - 620 С - небольшой эффект диссоциации образовавшегося карбоната магния. [30]
Страницы: 1 2 3 4