Гидроокись - кадмий
Cтраница 2
У гидроокиси кадмия отчетливо выражены лишь основные свойства. В кислотах обе гидроокиси легко растворяются. [16]
Получить гидроокись кадмия и испытать ее растворимость аналогично предыдущему. [17]
Обычно гидроокись кадмия получают осаждением из солеи растворами щелочей. Образующийся осадок легко кристаллизуется в такой же решетке, как и гидроокись магния. [18]
Окись и гидроокись кадмия и окись ртути обладают основными свойствами. Гидроокись ртути получить не удается, так как она распадается на окись ртути и воду. [19]
Окись и гидроокись кадмия легко растворимы в кислотах и растворимы в едких щелочах. [20]
Удельная поверхность гидроокиси кадмия с повышением рН и температуры возрастает от 4 до 15 м2 / г. Так как одновременно наблюдается снижение содержания NOJT, то увеличение поверхности может быть связано с уменьшением количества анионов. [21]
Требования, предъявляемые к гидроокиси кадмия особой чистоты, делали маловероятной возможность применения в данном случае в качестве осадителя едких щелочей. [22]
Вычислите, сколько миллиграммов гидроокиси кадмия может раствориться в 4 мл 1 5 М раствора аммиака. [23]
Вычислите, сколько миллиграммов гидроокиси кадмия может раствориться ( при условии полного растворения), в 4 мл 1 5 М раствора аммиака. [24]
Реакции ( заимодействия окиси или гидроокиси кадмия с пиррфосфатом салия подобны указанным выше для получения пирофрсфатного комплекса цинка. [25]
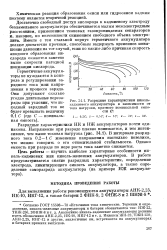 |
Разрядные характеристики никель-кадмиевого аккумулятора в зависимости от тока нагрузки, кратного номинальной емкости С. [26] |
Химическая реакция образования окиси или гидроокиси кадмия поэтому является вторичной реакцией. [27]
В разбавленных же растворах щелочей гидроокись кадмия практически не растворяется. [28]
В первой выпадает белый осадок гидроокиси кадмия, во второй - осадок, легко растворяющийся в избытке реактива, при этом образуется бесцветный раствор. [29]
Едкая щелочь осаждает белый осадок гидроокиси кадмия Cd ( OH) 2, не растворяющийся в избытке щелочи, но легко растворяющийся в кислотах, избытке аммиака, цианидах щелочных металлов. [30]
Страницы: 1 2 3 4