Гидроокись - кадмий
Cтраница 3
NH - С6Н4 - NO2) Гидроокись кадмия окрашивается при прибавлении реактив в бурый цвет. В присутствии формалина окраска делается сиш зеленой. [31]
Напишите уравнения реакций получения окиси и гидроокиси кадмия, на какие ионы диссоциирует в водном растворе гидроокись кадмия. [32]
Едкие щелочи выделяют белый студенистый осадок гидроокиси кадмия, нерастворимый в избытке реагента, но легко растворяющийся в кислотах, аммиаке и цианиде калия или натрия; хлорид аммония, лимонная и винная кислоты препятствуют осаждению. [33]
 |
Схема уста новки для получения фольговой основы электродов. [34] |
Аналогичный процесс предложен для пропитки отрицательных пластин гидроокисью кадмия. [35]
В щелочных растворах ограничение функции электрода связано с образованием гидроокиси кадмия. [36]
Оранжево-желтый сульфид образуется при длительном пропускании сероводорода через взвесь гидроокиси кадмия. [37]
У разов, Киракосян А. К. Изучение реакции между сульфатом и гидроокисью кадмия. [38]
Эти авторы показали, что ионы хлора, адсорбированные гидроокисью кадмия, уменьшают способность полученных растворов к растворению целлюлозы и что растворение гидроокиси кадмия при 0 С приводит к получению растворов с повышенной концентрацией кадмия в растворе. Однако более простой метод получения комплекса состоит в растворении окиси кадмия при комнатной температуре. На рис. II.3 приведены данные о растворимости целлюлозы в растворах кадоксена различного состава, приготовленных из окиси и гидроокисей кадмия, содержащих адсорбированные ионы хлора. [39]
Молибден отделяют от кадмия обработкой щелочью; при этом осаждается гидроокись кадмия. Для отделения кадмия от индия и редкоземельных элементов последние выделяют с гидроокисью железа, осаждаемой из раствора аммиаком. [40]
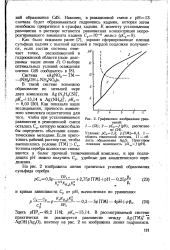 |
Графическое изображение уравнений. 7 - ( 23. 2 - рСр / ( рН, рассчитано. [41] |
Наконец, в реакционной смеси с рН13 сначала будет образовываться гидроокись кадмия, которая затем неизбежно превратится в сульфид кадмия. [42]
Гидроокись цинка Zn ( OH) 2 - амфотерное соединение, гидроокись кадмия Cd ( OH) 2 обладает основными свойствами со слабо выраженной кислотной функцией, гидраты же окислов Hg ( OH) a и Hg2 ( OH) 2 - неустойчивые соединения. [43]
В два последовательно соединенных поглотительных прибора наливают по 1 мл суспензии гидроокиси кадмия и по 4 мл воды. Для определения разовой концентрации исследуемый воздух со скоростью 2 л / мин протягивают в течение 20 - 30 мин. [44]
Готовят из тиоацетамида, который количественно гидролизу-ется до сульфида в присутствии гидроокиси кадмия. [45]
Страницы: 1 2 3 4