Гидроокись - магний
Cтраница 4
Гидроокись магния практически нерастворима и тоже выпадает в осадок. [46]
Гидроокись магния отфильтровывают, отмывают на фильтре водой и прокаливают при невысокой температуре для перевода в MgO. Сырьем для этого способа, помимо концентрированных растворов, может служить и морская вода. В зависимости от концентрации растворов, режима осаждения гидроокиси, промывки и прокаливания получаются различные сорта магнезии. [47]
Гидроокись магния растворима в кислотах и в растворах солей аммония. [48]
 |
Влияние содержания хлорид-ионов на удельную поверхность образцов, полученных осаждением из треххлористой сурьмы. [49] |
Гидроокись магния может быть использована в качестве полупродукта для получения катализаторов, например медно-магниевого, для конверсии окиси углерода [59], активной окиси магния и др. Обычно гидроокись магния получают осаждением из растворов солей магния растворами щелочей. Образующийся осадок имеет кристаллическую структуру. [50]
Гидроокись магния характеризуется большой адсорбционной способностью ( см. стр. Mg ( OH) 2 с красителем обычно иная, чем окраска красителя в растворе. [51]
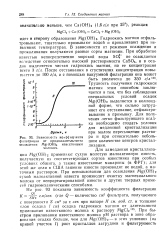 |
Зависимость коэффициента. [52] |
Гидроокись магния отфильтровывают, тщательно промывают водой и прокаливают при невысоких температурах. В зависимости от режимов осаждения и прокаливания получаются разные сорта магнезии. [53]
Гидроокись магния, полученная при одночасовом приливании известкового молока, хорошо отстаивается, через 2 - 4 ч после осаждения легко отмывается о т иона хлора и содержит 0 08 - 0 1 % Са. При вливании раствора магниевой соли в щелочь частицы осадка представляют собой студенистые образования. [54]
Гидроокись магния Mg ( OH) 2 выделяется при действии щелочей на растворы солей магния в виде объемистого студенистого осадка. Гидроокись магния - слабое основание, легко растворяется в кислотах, из воздуха поглощает углекислый газ. Растворимость ее в воде зависит от степени старения, для свежеосажденной гидроокиси магния составляет 7 0 - 10 - 4 моль. При прокаливании Mg ( OH) 2 постепенно переходит в MgO; последние следы воды из Mg ( OH) 2 удаляются с большим трудом. [55]
Гидроокись магния Mg ( OH) 2 представляет собой тонкоди сперсный белый порошок, получаемый обжигом природного минерала магнезита MgCO при 750 С. [56]
Гидроокись магния Mg ( OH) 2 в водном растворе образуется зри взаимодействии солей магния со щелочью или с аммиаком. [57]
Гидроокись магния Mg ( OH) 2 не выпадает в присутствии солей аммония, растворима в кислотах, но не растворима в избытке щелочи. [58]
Страницы: 1 2 3 4