Гидроокись - щелочной металл
Cтраница 2
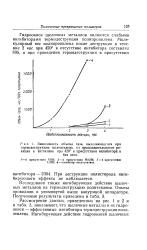 |
Зависимость объема газа, выделяющегося при термодеструкции полиэтилена, от продолжительности реакции в автоклаве при 420 в присутствии ингибитора и без него. [16] |
Гидроокиси щелочных металлов являются слабыми ингибиторами термодеструкции полипропилена. [17]
Гидроокиси щелочных металлов повышают электропроводность раствора, а гидроокись аммония способствует постоянству состава сплава при значительных изменениях плотностей тока и относительного содержания меди и цинка в растворе. Катодная плотность тока 0 2 - 3 А / дм2 в зависимости от содержания металлов в электролите и температуры электролита. При повышении плотности тока и понижении температуры электролита содержание меди в осадке уменьшается, выход по току на катоде резко падает. Анодная плотность тока не выше 1 А / дм2; при этом анодный выход по току приблизительно равен катодному. [18]
Гидроокиси щелочных металлов - сильные основания, основные свойства которых возрастают с увеличением атомного номера. [19]
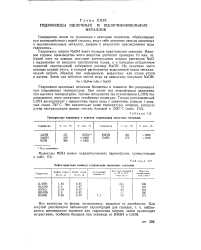 |
Температуры плавления и кипения гидроксидов щелочных металлов. [20] |
Гидроокиси щелочных металлов бесцветны и плавятся без разложения при повышенных температурах. Они кипят под атмосферным давлением при высоких температурах, причем испаряются ( за исключением LiOH) без разложения, имея достаточно устойчивые молекулы. Только расплавленный LiOH диссоциирует с выделением паров воды с давлением, равным 1 атм, уже около 750 С. [21]
Гидроокиси щелочных металлов, особенно гидроокись калия, при их плавлении более или менее обильно выделяют воду, что сопровождается вспениванием и разбрызгиванием; поэтому не следует смешивать анализируемую породу с плавнем до тех пор, пока расплав одного плавня не станет совершенно спокойным. [22]
Гидроокиси щелочных металлов и аммиак разлагают фторосиликаты на фториды и силикаты соответствующих металлов. [23]
Гидроокиси щелочных металлов образуют гидраты, которые могут быть получены в кристаллическом виде; например, КОН образует моно -, ди - и тетрагидраты. При комнатной температуре устойчив дигидрат, который в воде растворяется с поглощением тепла. Этим и объясняется приведенное выше изменение растворимости с температурой. [24]
Гидроокиси щелочных металлов, называемые также едкими щелочами, представляют собой бесцветные, очень едкие, довольно легкоплавкие массы. Следует отметить, что едкие щелочи в расплавленном состоянии сильно действуют не только на стеклянную и фарфоровую посуду, но при доступе воздуха также и на платину. [25]
Гидроокиси щелочных металлов очень хорошо растворимы в воде, причем растворение сопровождается значительным выделением тепла. Так, теплота растворения для NaOH составляет примерно 10 ккал / молъ. Гидроокиси щелочных металлов в водных растворах обычной концентрации почти полностью распадаются на ионы по уравнению МОН М - f - ОН, хотя коэффициенты электропроводности / ( i / u0 для мало разбавленных растворов вследствие действия межионных сил значительно ниже единицы. [26]
Гидроокиси щелочных металлов МОГУТ СЛУЖИТЬ в качестве превосходных осушителей для органических оснований, оставляя в них около 0 1 % воды. [27]
Получить гидроокись щелочного металла в результате реакции обмена можно, если образуется соль, растворимость которой меньше, чем исходной гидроокиси. [28]
Растворы гидроокисей щелочных металлов также вызывают оррозию олова, причем обыч-но образуются станнаты. При анодной коррозии могут также образовываться, ленки, приводящие к пассивированию. [29]
Из гидроокисей щелочных металлов практическое значение имеют едкий натр NaOH, известный под названием каустической соды, и едкое кали КОН. На аноде выделяется хлор, на катоде - водород, а в растворе образуется щелочь. [30]
Страницы: 1 2 3 4