Гидроокись - щелочной металл
Cтраница 4
 |
Приборы для перегонки растворителей. [46] |
Измельчение кусков гидроокисей щелочных металлов следует проводить за защитным стеклом, так как отлетающие мелкие кусочки очень опасны для глаз и волос. [47]
При прокаливании гидроокиси щелочных металлов проявляют заметную летучесть, которая возрастает от гидроокиси лития к гидроокиси цезия. [48]
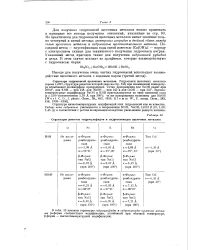 |
Структуры решеток гидросульфидов и гидроселенидов щелочных металлов. [49] |
Для получения гидроокисей щелочных металлов можно применять в принципе все методы получения оснований, указанные на стр. Но практически для гидроокисей щелочных металлов имеют значение только четвертый и пятый методы: электролиз хлоридов и двойной обмен между солью щелочного металла и гидроокисью щелочноземельного металла. Последний метод - каустификация соды едкой известью [ Са ( ОН) 2 ] - наряду с электролизом служит для технического получения гидроокиси натрия. Указанный метод пригоден также для получения гидроокисей рубидия и цезия. [50]
При добавлении гидроокиси щелочного металла к растворам Ag выпадает темно-коричневый осадок, который трудно отмыть от ионов щелочного металла. [51]
При применении гидроокисей щелочных металлов в эквимоль-ных количествах наиболее активными являются 8Э CsOH, NaOH и КОН. [52]
При применении гидроокисей щелочных металлов в эквимоль-ных количествах наиболее активными являются 89 CsOH, NaOH и КОН. [53]
Измельчение кусков гидроокисей щелочных металлов следует проводить за защитным стеклом, так как отлетающие мелкие кусочки очень опасны для глаз и волос. [54]
Кристаллическая структура гидроокисей щелочных металлов при комнатной температуре неизвестна. При более высокой температуре гидроокись калия имеет кубическую структуру хлорида натрия. Это обусловлено вращением ионов ОН в решетке, что и придает им сферическую симметрию ( см. аналогичное поведение ионов CN -, стр. Гидроокись лития LiOH обладает слоистой структурой ( стр. Li тетраэдрически окружен четырьмя ионами ОН, а каждая ОН - - группа притянута с одной стороны четырьмя ионами Li, а с другой - четырьмя ионами ОН соседнего слоя. В этих структурах ( даже у КОН) водородных связей между ОН - - груп-пами не существует. [55]
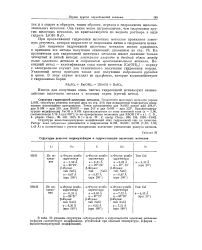 |
Структуры решеток гидросульфидов и гидроселенидов щелочных металлов. [56] |
При прокаливании гидроокиси щелочных металлов проявляют заметную летучесть, которая возрастает от гидроокиси лития к гидроокиси цезия. [57]
Страницы: 1 2 3 4