Гидроокись - висмут
Cтраница 3
Комплексообра-зователи, как, например, маннит в случае гидроокиси висмута [60] или ионы SO4 в случае гидроокиси циркония [111], препятствуют, в силу увеличения растворимости, образованию радиоколлоидов. Шуберт и Кон [111] исследовали радиоколлоидные свойства плутония и продуктов деления. [31]
Искомая соль должна состоять из одновалентных кислотных остатков соляной кислоты С1 и содержащих гидроксил основных остатков гидроокиси висмута. [32]
Томас и Смит [1296] выделяли висмут электролизом из сернокислых растворов сульфата, а также раствора, полученного растворением гидроокиси висмута в концентрированном растворе лимонной кислоты и добавлением NaOH до щелочной реакции. [33]
При разбавлении водой куприты разрушаются, выделяя осадок Си ( ОН) г. В концентрированных щелочах заметно растворяется и гидроокись висмута. Что касается белой Cd ( OH) 2 и желто HgO, то первая растворяется в них лишь в ничтожной степени, а вторая с щелочами практически не взаимодействует. [34]
Гидроокиси щелочных ( и щелочноземельных) металлов и аммиак осаждают из растворов солей висмута белые осадки, представляющие смесь гидроокиси висмута и соответствующих основных солей. [35]
Пятиокись висмута Bi20s имеет коричневый или темнокрасный цвет и получается обычно как окончательный продукт реа кции между хлором и гидроокисью висмута. Пятиокись висмута восстанавливается водородом при 215 в четырехокись, а при 255 в трехокись. При нагревании на воздухе или в кислороде при 250 пятиокись переходит в четырехокись, а при 300 в трехокись. При нагревании в вакууме до 100 пятиокись висмута полностью разлагается. [36]
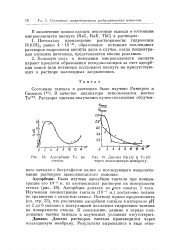 |
Диализ МЪ ( 7 и Та ( 2 через коллодиевую мембрану. [37] |
Поскольку произведение растворимости гидроокиси: Bi ( OH) 3 равно 4 10 - 81, образование истинных коллоидных растворов гидроокиси висмута даже в случае, когда концентрация элемента ничтожна, представляется вполне реальным. [38]
Следовательно, она очень невелика, и в аналитической практике, где мы обычно имеем дело с концентрациями растворов 0 1 - 0 01 М, можно принять, что гидроокись висмута не проявляет амфотерных свойств. [39]
NaOH или КОН, пока выпавший осадок Sn ( OH) 2 не растворится ( небольшая муть может оставаться, но раствор должен быть сильнощелочным-проба на лакмус), б) Получают осадок гидроокиси висмута, для чего на исследуемый раствор действуют избытком щелочи или аммиака, в) Полученный белый осадок обливают свежеприготовленным раствором станнита. В присутствии висмута осадок чернеет. [40]
В платиновой чашке нагревают 10 мл 40 % - ной водной плавиковой кислоты ( 0 2 моля) и 70 г 32 % - ного водного раствора фтористого аммония ( 0 61 моля) с 13 г ( 0 05 моля) гидроокиси висмута. Затем нагревание прекращают, при перемешивании прибавляют 24 5 г ( 0 15 моля) трехфтористого фенилкремния. Всплывающий на поверхность смеси маслянистый слой закри-сталлизовывается при охлаждении водой. Осадок отфильтровывают, высушивают, три-фенилвисмут извлекают эфиром. [41]
Метод разложения серной кислотой и персульфатом калия или серной кислотой и окисью хрома ( VI) 84, разработанный для определения галогенов в органических соединениях, был успешно применен для минерализации органических соединений мышьяка, сурьмы и висмута. Гидроокись висмута осаждают аммиаком из сернокислого раствора, отфильтровывают и после растворения в азотной кислоте определяют висмут в виде фосфата. [42]
С нарастанием металлических свойств при переходе от азота к нижним аналогам по подгруппе сила кислот в ряду HNO2, Н3РО3, H3AsO3, H3SbO3, H3BiO4 падает слева направо, однако даже азотистая кислота является лишь немного более сильной, чем уксусная. Гидроокись висмута Bi ( OH) 3 обладает преимущественно основными свойствами. [43]
Ее очень трудно получить в чистом состоянии, так как она, обладая коллоидной природой, легко адсорбирует кислотные ионы, которые прочно ею удерживаются. Очень легко гидроокись висмута получается в виде коллоидного раствора. Гидроокись висмута легко растворима в кислотах с образованием солей. В разбавленных щелочах она нерастворима. [44]
Убедитесь, что гидроокись висмута растворяется в кислотах, но не растворима в избытке щелочи. [45]
Страницы: 1 2 3 4