Гидроокись - фенилртуть
Cтраница 2
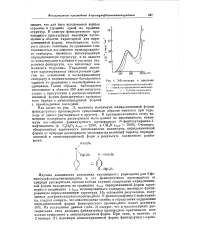 |
УФ-спектры в диоксане. [16] |
В спектре фенилртутного производного присутствует максимум поглощения в области, характерной для пири-дониминной формы, интенсивность которого сильно понижена по сравнению с интенсивностью поглощения метилированного стандарта, имеющего фиксированную пиридониминную структуру, и не зависит ог концентрации и добавки к раствору гидроокиси фенилртути, что исключает возможность гидролиза. Указанный максимум характеризуется гипсохромным сдвигом по отношению к метилированному стандарту и незначительным батохромным сдвигом по сравнению с незамещенным соединением. Таким образом, наблюдаемое поглощение в области 300 ммк свидетельствует о присутствии в растворе пиридон-иминной формы фенилртутного производного наряду с аминопиридинной формой с преобладанием последней. [17]
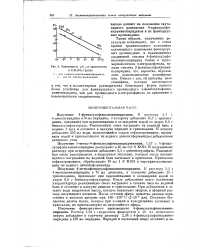 |
Зависимость рК от заместителя в CeHjSCyrpynne. [18] |
Раствор 2 94 г гидроокиси фенилртути в 40 мл метилового спирта добавляют к горячему раствору 2 34 г 4-фенилсульфониламинопиридина в 120 мл пиридина. [19]
Необходимые для проведения настоящего исследования окси - и мер-капто - К-гетероциклы синтезированы по описанным в литературе методикам и охарактеризованы по температурам плавления. Их металлоорга-нические производные получены при действии гидроокисей фенилртути, трифенилолова и трифенилсвинца, а также метилата триэтилолова на соответствующие гетероциклические системы. После смешения растворов металлоорганическои компоненты и окси - либо меркапто - К-гетероцикла в подходящем растворителе последний отгоняли и полученный остаток очищали кристаллизацией или перегонкой в вакууме. [20]
Для решения второй задачи в качестве растворителя был выбран нитрометан. Но оказалось, что при смешении нитрометана с гидроокисью фенилртути без освещения идет образование фенилнитрометилртути. [21]
Так же ведут себя арилы триарил-цианоборнатрия. Тетрафенилборнатрий с гидроокисью ртути в ацетоне дает дифенилртуть и гидроокись фенилртути [29, 31], с ацетатом ртути. [22]
Далее будет показано, что внутримолекулярно происходит также и гемолитический распад промежуточных соединений, образующихся при восстановлении солей диазония щелочным раствором формальдегида или при окислении фенилгидразина ( см. стр. Этот же гемолитический, скрыторадикальный механизм рассматривался применительно к реакции распада нитрозоацилариламинов [516], фоторазложения гидроокиси фенилртути [343] и др. Реакции окисления-восстановления, широко распространенные в биологических системах [611], также имеют, можно думать, аналогичный механизм, причем в этих случаях акцепторами и донорами водорода должны быть энзимы ( см. дополнение 14 на стр. [23]
Необходимым условием для этого является достаточная кислотность N - Н - связи, возникающая за счет электроноакцепторного эффекта соответствующих заместителей в ароматическом кольце, при отсутствии которого арилртутные производные не образуются. Так, в отличие от п-нитроанилина [1], анилин, и-хлор - и п-броманилины в аналогичных условиях не реагируют с гидроокисью фенилртути. [24]
Метил-4 5-дихлоримидазол получен хлорированием 2-метил-имидазола, а 4 7-дихлорбензимидазол - конденсацией 3 6-дихлор - 1 2-фенилендиамина с муравьиной кислотой. Фенилртутные производные синтезированы действием гидроокиси фенилртути на соответствующие гетероциклы. [25]
Из охлажденного раствора выделяется белый осадок гидроокиси фенилртути, который отмывается от щелочи холодной водой, перекристал-лизовывается из горячей воды и высушивается в эксикаторе. Упариванием фильтрата можно дополнительно получить 1 5 - 2 г гидроокиси фенилртути. [26]
Фенилнитрометилртуть с выходом 78 % получается при добавлении нитрометана к спиртовому раствору гидроокиси фенилртути. [27]
При попытке синтеза арилртутных производных N-замещенных пик-рамидов найдено, что при действии гидроокиси фенилртути на N-метил -, N-бензил - и N-фенилпикрамид не удается получить соответствующих производных. В ходе проведенного нами исследования установлено, что потеря способности к образованию арилртутных производных при взаимодействии с гидроокисью арилртути характерна и для ряда других соединений, содержащих кислотную N - Н - группу. Так, в отличие от незамещенных в аминогруппе нитроанилинов [1 ] не реагируют с гидроокисью фенилртути такие соединения, как 4-нитро - 2 4 - и 4 4-динитродифенил-амин, N-метил - и N-фенил-и - нитрозоанилин, 4-метиламиноазобензол и N-метил - 4-нитроанилин. В противоположность ацетамиду [4], бензамиду [4] и трихлорацетамиду не образуют фенилртутных производных ацетанилид, бензанилид, N-метилбензамид, а также / г-нитроацетанилид и анилид три-хлоруксусной кислоты. Не вступают в реакцию N-арилмеркурирования, в отличие от соответствующих 4-нитрофенилгидразонов, 2 4-динитрофенил-гидразоны бензальдегида, пропионового альдегида и бензофенона. [28]
В нагретый на водяной бане раствор 12 г уксуснокислой фенилртути в 1 л изопропиловаго спирта постепенно приливают 10 мл 30 % - ного раствора едкого кали. Нагревание продолжают еще 1 час, после чего раствор разбавляют равным объемом воды. Растворитель отгоняют от профильтрованного раствора примерно до остаточного объема 200 мл. При охлаждении выделяются кристаллы гидроокиси фенилртути, которую перекристаллизовывают из горячей воды. [29]
Страницы: 1 2