Гидроокись - цезий
Cтраница 2
Перекись цезия, Cs202, получают при пропускании сухого кислорода через свежеприготовленный раствор металлического цезия в жидком аммиаке, а также, нагревая в алюминиевом тигле металлический цезий в атмосфере сухого кислорода. Светло-желтые кристаллы Cs202 с плотностью 4 25 г / см3 плавятся при 400 - 450; с водой они образуют перекись водорода и гидроокись цезия. [16]
Сильно основной характер гидроокиси таллия ( I) соответствует общему правилу, что окислы и гидроокиси, отвечающие низшим степеням окисления элементов, всегда имеют более основной ( или менее кислый) характер, чем соответствующие высшим степеням окисления. Уменьшение кислотных свойств при переходе от борного ангидрида к окиси алюминия и связанное с этим увеличение основного характера объясняются теми же причинами, что и возрастание основного характера при переходе от гидроокиси лития к гидроокиси цезия и от гидроокиси бериллия к гидроокиси бария. [17]
Сильно основной характер гидроокиси таллия ( 1) соответствует общему правилу, что окислы и гидроокиси, отвечающие низшим степеням окисления элементов, всегда имеют более основной ( или менее кислый) характер, чем соответствующие высшим степеням окисления. Уменьшение кислотных свойств при переходе от борного ангидрида к окиси алюминия и связанное с этим увеличение основного характера объясняются теми же причинами, что и возрастание основного характера при переходе от гидроокиси лития к гидроокиси цезия и от гидроокиси бериллия к гидроокиси бария. Ионы элементов главной подгруппы III группы с зарядом 3 в своих гидроокисях сильно притягивают ионы кислорода и сравнительно столь же сильно отталкивают ионы водорода. Это и происходит в том случае, если объем центрального иона невелик. Отталкивающим действием трехзарядного положительного иона бора на ионы водорода объясняется также неспособность бора к существованию в водном растворе в виде свободного положительного иона. [18]
Сильно основной характер гидроокиси таллия ( I) соответствует общему правилу, что окислы и гидроокиси, отвечающие низшим степеням окисления элементов, всегда имеют более основной ( или менее кислый) характер, чем соответствующие высшим степеням окисления. Уменьшение кислотных свойств при переходе от борного ангидрида к окиси алюминия и связанное с этим увеличение основного характера объясняются теми же причинами, что и возрастание основного характера при переходе от гидроокиси лития к гидроокиси цезия и от гидроокиси бериллия к гидроокиси бария. [19]
Представлялось необходимым прежде всего детально изучить спектры самого БАМБФ. На рис. 6 представлены ИК-спектры в области валентных колебаний ОН для растворов в четыреххлористом углероде 0 40 М БАМБФ и 0 40 М БАМБФ - 0 10 М Д2ЭГФК; последний титровали до конечной точки Д2ЭГФК гидроокисью цезия. Введение Д2ЭГФК в раствор БАМБФ интенсифицирует полосу поглощения Н - связанного фенола и снижает ее частоту, что означает большее число связей и большую силу связи. [20]
Активность многих соединений цезия проявляется в их каталитической способности. Установлено, что при получении синтола ( синтетической нефти) из водяного газа и стирола из этилбензола, а также при некоторых других синтезах добавление к катализатору незначительного количества окиси цезия ( вместо окиси калия) повышает выход конечного продукта и улучшает условия процесса. Гидроокись цезия служит превосходным катализатором синтеза муравьиной кислоты. С этим катализатором реакция идет при 300 С без высокого давления. Металлический цезий лучше, чем другие щелочные металлы, ускоряет реакцию гидрогенизации ароматических углеводородов. [21]
Активность многих соединений цезия проявляется в их каталитической способности. Установлено, что при получении синтола ( синтетической нефти) из водяного газа и стирола из этилбензола, а также при некоторых других синтезах добавление к катализатору незначительного количества окиси цезия ( вместо окиси калия) повышает выход конечного продукта и улучшает условия процесса. Гидроокись цезия служит превосходным катализатором синтеза муравьиной кислоты. С этим катализатором реакция идет при 300 С без высокого давления. [22]
Действуя фтором или хлором на окись цезия, нагретую до 150 - 200, получают галогениды цезия. Окись цезия бурно реагирует с водой и медленнее со спиртом. С жидким аммиаком окись цезия образует амид и гидроокись цезия. [23]
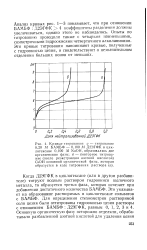
Анализ кривых рис. 1 - 3 показывает, что при отношении БАМБФ: Д2ЭГФК 4 коэффициенты разделения должны увеличиваться, однако этого не наблюдалось. Эти кривые титрования напоминают кривые, полученные с гидроокисью цезия, и свидетельствуют о незначительном отделении больших ионов от меньших. [25]
Таким образом, результаты исследований свидетельствуют об увеличении концентрации электронов в межэлектродном пространстве под действием фосфора. В обсуждении авторы обращают внимание на существующие экспериментальные доказательства присутствия в пламени как нейтральных атомов, так и гидроокиси, цезия, которые находятся в некотором равновесии. Возможно, что фосфор или галоиды нарушают равновесие между Cs и CsOH, активизируя ионизацию. Гидроокись цезия реагирует с водородом. В результате образуется цезий и вода. [26]
Из лепидолитов цезий извлекается вместе с рубидием попутно, как побочный продукт производства лития. Лепидолиты предварительно сплавляют ( или спекают) при температуре около 1000 С с гипсом или сульфатом калия и карбонатом бария. В этих условиях все щелочные металлы превращаются в легкорастворимые соединения - их можно выщелачивать горячей водой. После выделения лития остается переработать полученные фильтраты, и здесь самая трудная операция - отделение цезия от рубидия и громадного избытка калия. В результате ее получают какую-либо соль цезия - хлорид, сульфат или карбонат. Чтобы понять всю сложность последнего этапа, достаточно указать, что первооткрывателю цезия - крупнейшему немецкому химику Бунзену - так и не удалось получить элемент № 55 в свободном состоянии. Все способы, пригодные для восстановления других металлов, не давали желаемых результатов. Однако барий загрязнял конечный продукт, а работать с цианидами было трудно ввиду их крайней токсичности, да и выход цезия был весьма мал. Более рациональный способ найден в 1890 г. известным русским химиком Н. Н. Бекетовым, предложившим восстанавливать гидроокись цезия металлическим магнием в токе водорода при повышенной температуре. Водород заполняет прибор и препятствует окислению цезия, который отгоняется в специальный приемник. Однако и в этом случае выход цезия не превышает 50 % теоретического. [27]
Страницы: 1 2