Гидроокись - галлий
Cтраница 3
При ( растворении гидроокиси галлия в растворах молочной, винной, лимонной и щавелевой кислот образуются соли, которые могут быть выделены из растворов в виде кристаллогидратов. [31]
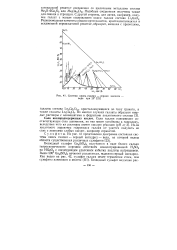 |
Система окись галлия - серная кислота - вода при 20. [32] |
Из-за кислотного характера гидроокиси галлия не удается получить ее соль с анионами слабых кислот, например сернистой. [33]
Ввиду значительной растворимости гидроокиси галлия в избытке аммиака необходимо очень тщательно регулировать прибавление его к раствору. [34]
Сравнительная медленность дегидратации гидроокиси галлия и перехода ее в более бедную водой плотную форму вызывает повышенную адсорбционную способность ее в отношении других катионов, присутствующих в растворе, хотя и не осаждающихся в отдельности при данных условиях. [35]
Метод основан на способности гидроокиси галлия растворяться в избытке едкой щелочи. [36]
Нагревание раствора после осаждения гидроокиси галлия пиридином приводит к дегидратации последней с переходом ее в более плотную форму, растворимость которой гораздо ниже. [37]
Так как плотная форма гидроокиси галлия имеет тенденцию плотно приставать к стенкам сосуда, то ее выделение целесообразно проводить в присутствии мацерированной бумаги. [38]
Нагревание раствора после осаждения гидроокиси галлия пиридином приводит к дегидратации последней с переходом в более плотную форму, растворимость которой гораздо ниже. [39]
Окись 1п2О3 получают, прокаливая гидроокись галлия или его нитрат. Она светло-желтая, приобретает при нагревании коричневую окраску. Легко растворяется в кислотах, если не была подвергнута сильному и продолжительному прокаливанию. Прокаленная окись индия на холоду реагирует с кислотами очень медленно, но хорошо растворяется в разбавленных кислотах при нагревании. Щелочи на нее не действуют. При 700 - 800 восстанавливается водородом или углеродом до металла. [40]
Окись 1п2О3 получают, прокаливая гидроокись галлия или его нитрат. Она светло-желтая, приобретает при нагревании коричневую окраску. Легко растворяется в кислотах, если не была подвергнута сильному и продолжительному прокаливанию. Прокаленная окись индия на холоду реагирует с кислотами очень медленно, но хорошо растворяется в разбавленных кислотах при нагревании. Щелочи на нее не действуют. При 700 - 800 восстанавливается водородом или углеродом до металла. [41]
Являясь идеальным примером амфотерности, гидроокись галлия легко растворима в избытке щелочей с образованием галла-тов. Гидроокись галлия также растворима в избытке аммиака, повидимому с образованием растворимого галлата аммония. [42]
Фрикке и Меринг [815] считают гидроокись галлия идеальным амфотерным водным окислом. Этот вывод делается ими на основании рассчитанных величин вторых и третьих констант диссоциации гидроокиси по кислотному и основному типам, имеющим очень близкие значения. [43]
Как показали опыты, осаждение гидроокиси галлия пиридином в присутствии марганца, кобальта, никеля, меди не приводит к достаточно полному разделению вследствие того, что гидроокись галлия, обладая амфотерными свойствами, образует с указанными металлами галлаты, которые загрязняют выделяющуюся гидроокись галлия. Это особенно отчетливо проявляется при осаждении гидроокиси галлия в присутствии кобальта. [44]
Как показали опыты, осаждение гидроокиси галлия пиридином в присутствии марганца, кобальта, никеля, меди не приводит к достаточно полному разделению. [45]
Страницы: 1 2 3 4