Малорастворимая гидроокись
Cтраница 3
IV); в области более низких концентраций НС1О4 процесс осложняется из-за выпадения осадка малорастворимой гидроокиси индия. [31]
Действие этого индикатора основано на том, что трехвалентный таллий образует с ионами гидроксила темно-бурую малорастворимую гидроокись Т1 ( ОН) 3, остающуюся в растворе в коллоидном состоянии и окрашивающую его в желтый цвет. Переход окраски от бесцветной к желтой хорошо заметен. Этот индикатор применим при титровании растворов, содержащих сильные окислители. [32]
Однако, когда мы имеем дело с весьма важными для промышленной и аналитической практики малорастворимыми гидроокисями, карбонатами и сульфидами, следует обязательно учитывать весьма слабую их диссоциацию в водных растворах. [33]
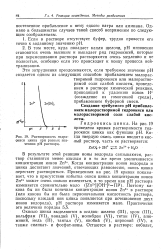 |
Растворимость гидроокиси цинка при разных значениях рН раствора. [34] |
Эти затруднения преодолеваются, если требуемое значение рН создается одним из следующих способов: прибавлением малорастворимой гидроокиси или малорастворимой соли слабой кислоты, проведением в растворе химической реакции, приводящей к удалению ионов Н ( осаждение из гомогенной среды), прибавлением буферной смеси. [35]
Если добавлять щелочь к растворам солей, то при достижении определенных рН может начаться выпадение малорастворимых гидроокисей металлов. [36]
Задачей исследования было выяснение поведения ряда ионов при осаждении из растворов, содержащих эти ионы, малорастворимых гидроокисей. [37]
Метод определения железа по реакциям Fe2 pt Fe3 1 е с концентрированием элемента а электроде в виде малорастворимой гидроокиси отличается от методов классической полярографии гораздо более высокой чувствительностью и избирательностью. [38]
В аналитической практике, несмотря на определенные недостатки, по-прежнему находит широкое применение метод соосаждения примесей с малорастворимыми гидроокисями металлов в аммиачно-щелочной среде. [39]
Наряду с образованием сульфидов для разделения ионов в количественном анализе широко применяется также осаждение различных катионов в виде малорастворимых гидроокисей. При этом для разделения ионов используют либо амфотерность некоторых из них, либо различия в растворимости разных гидроокисей. Так, железо отделяют от ванадия, молибдена и алюминия, обрабатывая раствор избытком едкой щелочи. [40]
Следовательно, магний легко растворяется при анодной поляризации в кислых и нейтральных растворах, но пассивируется за счет образования малорастворимой гидроокиси в щелочных растворах. Накопление в прианодном пространстве водородных ионов при ЭХО в слабощелочных растворах или при отсутствии буферирования может привести к повышению растворимости пассивирующей пленки и переходу металла в раствор. [42]
Этот путь концентрирования связан с электрохимической переменой валентности определяемого иона, не дающего в данных условиях в данной среде малорастворимой гидроокиси. [43]
Особенно много внимания было уделено определению никеля в присутствии других элементов, образующих с KCN осадки, комплексные соединения или малорастворимые гидроокиси. Если на такой раствор подействовать бромной водой, то кобальт перейдет в соединение [ Со ( CN) e ] 3 -, а никель выпадает в виде Ni ( OH) 3; осадок отделяют от раствора, растворяют в щавелевой кислоте, подщелачивают раствор аммиаком и вновь титруют раствором KCN. [44]
Нейтральность реакционной среды достигается нейтрализацией образующегося во время реакции едкого кали двуокисью углерода или путем добавления солей магния или алюминия, которые образуют слабощелочные малорастворимые гидроокиси. Полная нейтральность реакционной среды достигается применением в качестве окислителя перманганата магния или перманганата цинка, однако эти реагенты дороги и трудно доступны. [45]
Страницы: 1 2 3 4
