Остальная гидроокись
Cтраница 1
Остальные гидроокиси, к которым относятся серо-зеленый гидрат окиси хрома Сг ( ОН) 3, красно-коричневый гидрат окиси железа Fe ( OH) 3 и светло-зеленый гидрат закиси Ni ( OH) 2 на воздухе практически не изменяются. [1]
Остальные гидроокиси, к которым относятся серо-зеленый гидрат окиси хрома Сг ( ОН) з, красно-коричневый гидрат окиси железа Fe ( OH) 3 и светло-зеленый гидрат закиси никеля Ni ( OH) 2 на воздухе практически не изменяются. [2]
Остальные гидроокиси, к которым относятся серо-зеленый гидрат окиси хрома Сг ( ОН) 3, красно-коричневый гидрат окиси железа Fe ( OH) 3 и светло-зеленый гидрат закиси Ni ( OH) 2 на воздухе практически не изменяются. [3]
Аналогичные величины получаются и для остальных гидроокисей щелочных металлов ( ср. [4]
 |
Схема цилиндроконического карбонизатора. [5] |
Часть гидроокиси возвращается на карбонизацию в виде затравки, остальная гидроокись является продукционной. Промывка продукционной гидроокиси обычно осуществляется на барабанных фильтрах с промежуточной репульпацией кека. В качестве затравки может быть использована тонкодисперсная часть гидроокиси, в этом случае ее классифицируют по крупности в гидроциклонах или других аппаратах. [6]
Это обусловлено, вероятно, сильными кулоновскими взаимодействиями небольшого иона Ве2 и прочными водородными связями между плотноупакованными ионами ОН - в Ве ( ОН) 2 ( кр) по сравнению с меньшими ( убывающими при возрастании Z) значениями соответствующих энергий у остальных гидроокисей щелочноземельных металлов. [7]
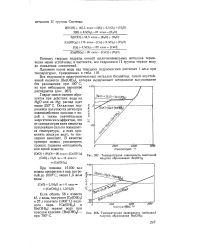 |
Температурная зависимость свободной энергии образования Ве ( ОН2.| Температурная зависимость свободно и энергии образования Ва ( ОН2. [8] |
Гидрат окиси магния образуется при действии воды на MgO или на Mg; распад идет выше 250 С. Остальные гидроокиси получаются легко при взаимодействии окислов с водой с таким значительным энергетически м эффектом, что от саморазогрев ания вещества при реакции силь но повышается температура, а если применять жидкую воду, то последняя закипает. [9]
Метод разложения испытуемых проб зависит от их природы. В обычном ходе анализа горных пород р.з.э. количественно выделяются аммиаком с остальными гидроокисями. При определении церия в горных породах из отдельной навески исходную навеску разлагают смесью 5 - 10 мл HF и 10 - 15 мл HaSO. После растворения всей навески удаляют ИР упариванием раствора до густых паров 5Оз, затем охлаждают, смывают края посуды водой и снова выпаривают, пока не останется 1 мл HuSO. По охлаждении приливают 50 мл холодной воды и при периодическом перемешивании оставляют на некоторое время, так как растворение сульфатов р.з.э. при высоком их содержании происходит медленно, особенно в нагретом состоянии. [10]
Прежде всего, он двухвалентен, тогда как ионы К, Na и NH4 одновалентны. Далее, гидроокись магния сравнительно мало растворима в воде, в то время как остальные гидроокиси металлов I группы растворимы весьма сильно. [11]
В соответствии с приведенным выше правилом кислотный характер гидроокисей в каждой главной подгруппе периодической системы уменьшается с возрастанием порядкового номера элемента. Это правило оправдывается и в данном случае: азотная кислота - очень сильная кислота, фосфорная - кислота средней силы, а остальные гидроокиси - все слабые или даже очень слабые кислоты. [12]
Полученная в результате декомпозиции гидратная пульпа состоит из выпавшей в осадок гидроокиси алюминия и маточного щелочного раствора. Гидроокись алюминия отделяют от маточного раствора сгущением; часть полученной гидроокиси алюминия возвращают в виде затравки в следующие порции раствора, идущего на декомпозицию, остальную гидроокись после фильтрации и промывки прокаливают ( кальцинируют) при высокой температуре. В результате прокаливания гидроокись алюминия обезвоживается и превращается в глинозем. [13]
На первой стадии производится обработка щелочью ( NaOH) до рН 4 5н - 4 0, при котором происходит осаждение Fe ( OH) 3 и основной массы ванадия, а на второй стадии процесс нейтрализации проводится при рН 8 5 - - 10, при котором осаждаются остальные гидроокиси. Вторая стадия осуществляется известью. В этом случае ценность представляет шлам, полученный на первой стадии нейтрализации. [14]
Ионы бора и алюминия сильно отличаются от ионов галлия, индия и таллия, хотя вместе они составляют подгруппу IIIA. В ( ОН) 3 проявляет кислые свойства, А. ОН) 3-амфотерное соединение и согласно правилу увеличения основных свойств в направлении сверху вниз ( вследствие увеличения радиусов ионов) следовало бы ожидать увеличения основных свойств у остальных гидроокисей элементов этой подгруппы. ОН) 3 основные свойства выражены слабо. Наружные оболочки ионов бора и алюминия напоминают оболочки благородных газов, а наружные оболочки ионов галлия и других элементов этой подгруппы обладают восемнадцатиэлектронной структурой. [15]
Страницы: 1 2