Остальная гидроокись
Cтраница 2
Это Свойство - в наиболее резкой форме выражено у Hg и Hg2, гидроокиси которых практически не существуют; гидроокись серебра легко отщепляет большую часть воды, превращаясь в окись; гидрат окиси меди теряет воду при нагревании. Столь же резко отличаются гидроокиси друг от друга и по своей электролитической характеристике. В качестве крайних случаев могут рассматриваться: сильное основание, AgOH, с одной стороны, и достаточно сильно ионизированная мышьяковая кислота - с другой. Для всех остальных гидроокисей в более или менее сильной степени характерны амфотерные свойства. Наиболее слабо выражена кислотная функция у Cd ( OH) 2 и Bi ( OH) 3, которые практически являются только основаниями. Наоборот, соответствующие производные трех - и пятивалентного мышьяка, пятивалентной сурьмы и четырехвалентного олова диссоциируют в растворах преимущественно по кислотному типу, а потому существование этих элементов в виде катионов возможно только в условиях достаточно кислой среды. [16]
Это свойство в наиболее резкой форме выражено у Hg и Hg2, гидроокиси которых практически не существуют-гидроокись серебра легко отщепляет большую часть воды, превращаясь в окись; гидрат окиси меди теряет воду при нагревании. Столь же резко отличаются гидроокиси друг от друга и по своей электролитической характеристике. В качестве крайних случаев могут рассматриваться: сильное основание, AgOH, с одной стороны, и достаточно сильно ионизированная мышьяковая кислота - с другой. Для всех остальных гидроокисей в более или менее сильной степени характерны амфотерные свойства. Наиболее слабо выражена кислотная функция у Cd ( OH) 2 и Bi ( OH) 3, которые практически являются только основаниями. [17]
Калий и натрий являются наиболее активными металлами из всех часто встречающихся электроположительных элементов ( стр. Они очень быстро окисляются на воздухе и разлагают воду при обыкновенной температуре; водород воды восстанавливается до газообразного состояния, а металл окисляется до гидроокиси. Гидроокиси щелочных металлов являются весьма сильными основаниями, что видно по степени их ионизации ( стр. В твердом виде они являются наиболее стойкими из всех остальных гидроокисей и не расщепляются на окись и воду даже при плавлении. Получение чистых окисей удается лишь с большим трудом; осторожное нагревание металлов на воздухе ведет к образованию наряду с окисью значительного количества перекиси. [18]
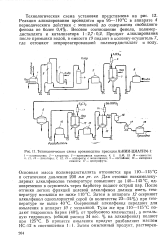 |
Технологическая схема производства присадки АзНИИ - ЦИАТИМ-1. [19] |
Основная масса полимердистиллята отгоняется при НО-115 С и остаточном давлении 200 мм рт. ст. Для отгонки низкомолекулярных алкилфенолов температуру повышают до 140 - 145 С, одновременно в осушитель через барботер подают острый пар. После отгонки легких фракций целевой алкилфенол должен иметь температуру вспышки не ниже 110 С. Затем в аппарате 12 осерняют алкилфенол однохлористой серой ( в количестве 23 - 24 %) при температуре не выше 40 С. Осерненный алкилфенол передают для омыления в аппарат 10 с мешалкой. Туда же при ПО-115 С подают гидроокись бария ( 40 % от требуемого количества), а остальную гидроокись ( общий расход 34 вес. [20]
Отвечающие катионам этой группы гидроокиси весьма сильно различаются по свойствам. Некоторые из них относительно устойчивы, другие, наоборот, настолько непрочны, что распадаются на соответствующий окисел и воду уже в момент образования. Это свойство в наиболее резкой форме выражено у Hg и Hg2, гидроокиси которых практически не существуют; гидроокись серебра легко отщепляет большую часть воды, превращаясь в окись; гидрат окиси меди теряет воду при нагревании. Столь же резко отличаются гидроокиси друг от друга и по своей электролитической характеристике. В качестве крайних случаев могут рассматриваться: сильное основание, AgOH, с одной стороны, и достаточно сильно ионизированная мышьяковая кислота - с другой. Для всех остальных гидроокисей в той или иной мере характерны амфотерные свойства. Наиболее слабо выражена кислотная функция yCd ( OH) 2 и Bi ( OH) 3, которые практически являются только основаниями. Наоборот, соответствующие производные трех - и пятивалентного мышьяка, пятивалентной сурьмы и четырехвалентного олова диссоциируют в растворах преимущественно по кислотному типу. [21]
Страницы: 1 2