Гидрооксид - кальций
Cтраница 2
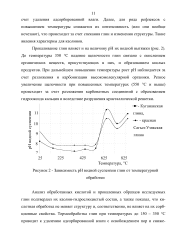 |
Зависимость рН водной суспензии глин от температурной. [16] |
До температуры 350 С падение щелочности глин связано с окислением органических веществ, присутствующих в них, и образованием кислых продуктов. При дальнейшем повышении температуры рост рН наблюдается за счет разложения и карбонизации высокомолекулярной органики. Резкое увеличение щелочности при повышенных температурах ( 550 С и выше) происходит за счет разложения карбонатных соединений с образованием гидрооксида кальция и вследствие разрушения кристаллической решетки. [17]
Вероятность образования гидросуль-фаталюмината также мала, так как в исходном вяжущем содержание алюминатов незначительно. Все это приводит к тому, что образование коррозионноопасных для камня продуктов происходит лишь в поверхностном слое и отсутствует внутри цементного камня. Наличие в поровой жидкости значительного количества ионов Na создает возможность катионного обмена между средой и продуктами твердения цементного камня, а именно гидрооксидом кальция, высокоосновными гидросиликатами и гидроалюминатами кальция. Катионный обмен происходит с образованием легко растворимых силикатов и алюминатов натрия, что вызывает увеличение пористости, проницаемости и снижения прочности цементного камня. [18]
По данным ( 1, 2 ] для углеродистой стали при консервации теплоэнергетического оборудования и котлов способностью защитить металла от коррозии обладает гидрооксид кальция. Из всех щелочных агентов, которые применяют в технике противокоррозионной защиты, Са ( ОН) 2 наиболее дешев и доступен. Более того, он является отходом ряда химических производств, т.е. в ряде случае использование Са ( ОН) 2 одновременно позволит решить проблему утилизации отходов Гидрооксид кальция безвреден для человека и окружающей среды, санитарных норм, ограничивающих сброс растворов Са ( ОН) 2 в природные водоемы, не установлено. [19]
По данным [1, 2] для углеродистой стали при консервации теплоэнергетического оборудования и котлов способностью защитить металла от коррозии обладает; гидрооксид кальция. Из всех щелочных агентов, которые применяют в технике противокоррозионной защиты, Са ( ОН) 2 наиболее дешев и доступен. Более того, он является отходом ряда химических производств, т.е. - в ряде случае использование Са ( ОН) 2 одновременно позволит решить проблему утилизации, отходов. Гидрооксид кальция безвреден для человека и окружающей среды, санитарных норм, ограничивающих сброс растворов Са ( ОН) 2 в природные водоемы, не установлено. [20]
Подробно рассмотрим влияние АРНК на процесс соле-отложения. АРНК является побочным продуктом производства минеральных удобрений. При взаимодействии АРНК с пластовой гидрокарбонатно-натриевой водой образуется карбонат кальция, формирующий твердый осадок на поверхности нефтепромыслового оборудования. Минералогическими методами установлено наличие в составе осадка гидрооксида кальция Са ( ОН) 2 коллоидной формы. [21]
Формирование ГШЦ-камня и ГПЩП-камня начинается и протекает сразу же после затворения вяжущего вещества водой. Происходит гидратация полуводного гипса с образованием кристаллов двуводного гипса. Одновременно протекают реакции взаимодействия портландцементного клинкера с водой. Возникающие новообразования вступают в контакт с гипсом, образуя кристаллы эттрин-гита. Игольчатые кристаллы эттрингита как бы армируют структуру камня, способствуют дополнительному уплотнению и упрочнению формирующегося каркаса из двуводного гипса в виде кристаллического сростка. Следует, однако, отметить, что щелочность среды в этот период понижена за счет взаимодействий свободного гидрооксида кальция с активным минеральным веществом в виде пуццолановых ( в ГЦПВ) или шлаковых ( в ГШЦПВ) добавок. Субмикроскопическая масса образует пространственную сетку экранирующих пленок вокруг кристаллов двуводного гипса и кристаллических новообразований, исходных частиц портландцемента и других дисперсных компонентов, цементируя их в общий микродисперсный конгломерат ГЦП-камень или ГШЦП-камень. [22]
Страницы: 1 2