Гидроперок-сида
Cтраница 1
Гидроперок-сиды легко разрушаются соединениями металлов переменной валентности, однако распад, как правило, протекает с образованием свободных радикалов; поэтому в присутствии кислорода эти катализаторы ускоряют окисление. Катализаторами гетеро-литического разложения ROOH являются кислоты Бренстеда. Гидропероксид кумила, в частности, распадается под действием кислоты на фенол и ацетон. [1]
В этих условиях хорошо определяются гидроперок-сиды трет-бутила и кумила, трет-бутилпербензоат, пе-роксид бензоила. Для ускорения восстановления перок - сида кумила реакцию ведут при 9О С. [2]
Аналогичные примеры известны и для ингибиторов, разрушающих гидроперок-сиды. [3]
По сходной схеме ароксилы реагируют с оксимами, гидроперок-сидами, тиолами и анилинами. [4]
На термическое разложение симметричных алкилпероксидов по сравнению с гидроперок-сидами полярность среды оказывает меньшее влияние. [5]
Это объясняется тем, что образующийся в условиях опытов гидроперок-сид н-децила ( ROOH) оказывает существенное влияние на скорость окисления н-декана. [6]
Экзотермичность реакции объясняется тем, что энергия образования О - Н - связи в гидроперок-сиде выше энергии разрыва С - Н - связи при бензильном атоме углерода. [7]
Ранее [1] было показано, что при использовании смешанного растворителя спирт - кумол существенно улучшаются показатели реакции эпоксидирования а-олефинов органическими гидроперок-сидами. Лучшие результаты были достигнуты при эпоксидирова-нии в присутствии вторичных спиртов. [8]
Радикалы RO2 - по мере накопления продуктов реакции реагируют не только с исходным веществом, но и с более реак-ционноспособными продуктами его превращения - гидроперок-сидами, спиртами, кетонами, сложными эфирами. [9]
Радикалы R02 - по мере накопления продуктов реакции реагируют не только с исходным веществом, но и с более реак-ционноспособными продуктами его превращения - гидроперок-сидами, спиртами, кетонами, сложными эфирами. [10]
Алюмогидрид лития восстанавливает все классы пероксидных соединений. Органические гидроперок-сиды гладко превращаются при комнатной температуре в соответствующие спирты с выделением 2 моль водорода на 1 моль гидро-пероксида; другие пероксидные соединения дают 1 моль водорода на 1 моль. Применимость данного восстановителя лимитируется помехами, которые создают другие группы, способные к восстановлению. Лишенный этого недостатка борогидрид натрия нашел пока лишь ограниченное применение. [11]
Алюмогидрид лития восстанавливает все классы пероксидных соединений. Органические гидроперок-сиды гладко превращаются при комнатной температуре в соотнес ствующие спирты с выделением 2 моль водорода на 1 моль гидро-пероксида; другие пероксидные соединения дают 1 моль водорода на 1 моль. Применимость данного восстановителя лимитируется помехами, которые создают другие группы, способные к восстановлению. Лишенный этого недостатка борогидрид натрия нашел пока лишь ограниченное применение. [12]
В настоящее время наиболее эффективным методом получения пропиленоксида, как уже отмечалось, является эпоксидиро-вание пропилена гидропероксидными соединениями. Для эпокси-дирования пропилена могут быть применены любые гидроперок-сиды, но на практике по ряду причин используют только гидро-пероксиды изобутана и этилбензола. Экономика этих процессов определяется по существу возможностями и ценами реализации побочных продуктов - 2-метилпропанола - 2 и стирола. ГПК в качестве эпоксидирующего агента за рубежом не используется. [13]
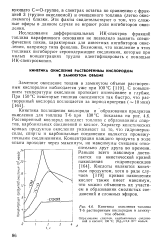 |
Кинетика окисления топлива Т-6 растворенным кислородом в замкнутом объеме. [14] |
Кинетика поглощения кислорода и образования продуктов окисления для топлива Т-6 при 130 С показана на рис. 4.6. Растворенный кислород окисляет топливо с образованием спиртов, карбонильных соединений и кислот. Характер кинетических кривых продуктов окисления указывает на то, что гидроперок-сиды, спирты и карбонильные соединения являются промежуточными соединениями. Концентрация каждого продукта в ходе опыта проходит через максимум, но максимумы смещены относительно друг друга во времени. [15]
Страницы: 1 2