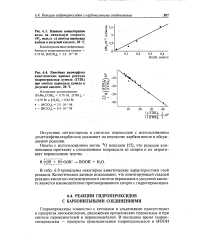
Гидропероксид
Cтраница 2
Гидропероксиды обладают более сильными кислотными свойствами, чем спирты. Так, с концентрированными растворами щелочей они образуют соли. Гидропероксиды являются окислителями, например легко реагируют с йодистым водородом, выделяя при этом иод. [16]
Гидропероксиды восстанавливаются до спиртов алюмогид-ридом лития, трифенилфосфином [558] или при каталитическом гидрировании. [17]
Гидропероксид, являясь сильным окислителем, способен сам окислять и разрушать целлюлозу. С другой стороны, в присутствии плат гидропероксид может выделять перекись водорода, которая также является сильным окислителем целлюлозы. [18]
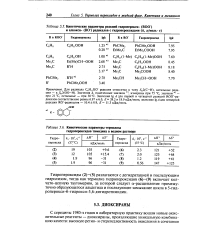 |
Кинетические параметры реакций гидроперокси - ( ROO.| Кинетические параметры термолиза. [19] |
Гидропероксиды ( 2) - ( 5) разлагаются с дегидратацией и последующим гидролизом, тогда как термолиз гидропероксидов ( 6) - ( 9) включает кол-чато-цепную таутомерию, за которой следует сс-расщепление промежуточно образующегося альдегида и последующее замыкание цикла в 5-гид-роперокси - 6-гидрокси - 5 6-дигидротимидин. [20]
Гидропероксиды совместно с кетонами и альдегидами присутствуют в продуктах автоокисления, разложения органических пероксидов и при синтезе пероксикеталей и пероксиацеталей. [22]
Гидропероксиды относятся к числу довольно нестабильных соединений, превращающихся при окислении в другие продукты. Поэтому их концентрация в реакционной массе, особенно при каталитическом окислении или при повышенных температурах, невелика. [23]
Гидропероксиды при разложении под действием повышенной температуры или катализаторов окисления действительно дают спирты и карбонильные соединения. Это разложение может иметь молекулярный механизм, однако в развившемся процессе окисления продукты образуются главным образом цепным путем. [24]
Гидропероксиды - слабые к-ты и дают соли со щелочными и щел. [25]
Гидропероксиды реагируют с двойной связью. [26]
Гидропероксиды и дистаннилпероксиды ( при нагревании взрываются. [27]
Гидропероксиды являются малостабильными веществами и легко разлагаются, особенно при контакте с нагретыми металлическими поверхностями. На примере изомерных пентил -, гек-сил - и гептилгидропероксидов было показано, что относительная стабильность М - уменьшается в ряду 3 - 2 - 1 - гидро-пероксиды, а также пентил-гексил-гептилгидропероксиды. Вероятность выброса НО2 из М уменьшается в таких же рядах. [28]
Гидропероксиды, образующиеся при окислении алкенов, являются, как правило, нежелательными побочными продуктами. [29]
Гидропероксиды и пероксиды способны легко взрываться. [30]
Страницы: 1 2 3 4