Гидросульфид - аммоний
Cтраница 1
Гидросульфид аммония NH4H S - белый кристаллический порошок, хорошо растворимый в воде и спирте и нерастворимый в эфире и бензоле. На воздухе легко разлагается. Хранить его нужно в запаяппой ампуле. [1]
Сульфиды и гидросульфиды аммония являются нестойкими соединениями и при нагревании до температуры более 90 С распадаются на сероводород и аммиак, основную массу которых относительно легко можно выделить из раствора. Поскольку сероводород более летуч, чем аммиак, он быстрее и полнее выделяется из раствора, и рН технологического конденсата повышается. [2]
Продуктом этой реакции является гидросульфид аммония. [3]
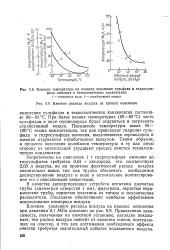 |
Влияние температуры на полноту окисления сульфида и гидросульфида аммония в технологических конденсатах.| Влияние расхода воздуха на процесс окисления. [4] |
Теоретически на окисление 1 г гидросульфида аммония до тиосульфатов требуется 0 63 г кислорода, что соответствует 2 03 л воздуха, но на практике фактический расход воздуха значительно выше, так как трудно обеспечить необходимое диспергирование воздуха в воде и оптимальное контактирование его с окисляемыми веществами. [5]
Однако в конденсатах находятся сульфиды и гидросульфиды аммония, которые при нагревании распадаются на сероводород и аммиак. Их содержание колеблется от десятков до нескольких тысяч миллиграммов на литр, поэтому технологический конденсат можно использовать на ЭЛОУ только после специальной очистки, например, отдувки из него сероводорода и аммиака водяным паром или углеводородным газом. [6]
Однако в этих конденсатах находятся сульфиды и гидросульфиды аммония, которые при нагревании распадаются на сероводород и аммиак. Их содержание колеблется от десятков до нескольких тысяч миллиграммов на литр, поэтому технологический конденсат можно использовать на ЭЛОУ только после специальной очистки. [7]
Были исследованы следующие восстановители: дисульфид натрия, гидросульфид аммония, хлористое олово с соляной кислотой, фенилгидра-зин, формальдегид, цинк и железо с соляной кислотой, цинк с хлористым кальцием, цинк с едким натром, гидросульфид натрия; применяли также электрохимическое восстановление. Во всех этих случаях восстановления почти не происходит, что, по-видимому, связано с тем, что в этих средах полинитросополимер не набухает. [8]
Метод ректификации также основан на свойстве сульфида и гидросульфида аммония разлагаться при нагреве с выделением сероводорода и аммиака. Раздельное получение чистого сероводорода и чистого аммиака вполне объяснимо, так как эти вещества имеют различные температуры кипения ( - 33, 35 С для сероводорода и - 60 7 С для аммиака) и, значит, разные упругости паров при любой заданной температуре. [10]
Метод ректификации также основан на свойстве сульфида и гидросульфида аммония разлагаться при нагреве с выделением сероводорода и аммиака. Раздельное получение чистого сероводорода и чистого аммиака вполне объяснимо, так как эти вещества имеют различные температуры кипения - 33, 35 С для сероводорода и - 60 7 С для аммиака) и значит разные упругости паров при любой заданной температуре. [11]
Сероводород в абсорбере абсорбируется поглотительным раствором с образованием гидросульфида аммония. При регенерации растворителя гидросульфид аммония окисляется до серы контактом с воздухом. Серу, выделяющуюся в виде пены, всплывающей на поверхность жидкости в окислительном реакторе, отделяют фильтрацией и направляют на дальнейшую переработку. [12]
Аналогичная 3 6-дегидроциклизация наблюдается при омылении тринит-рата целлюлозы гидросульфидом аммония. [13]
Уже при 20 давление диссоциации составляет 355 мм рт. ст. Гидросульфид аммония в значительной степени распадается и в водном растворе. [14]
В растворе накопляются и нерегенерируемые соли, образующиеся в результате окисления гидросульфида аммония, образования продуктов взаимодействия компонентов раствора с цианистым водородом, а также при омылении цианистого водорода. Как правило, эти процессы более интенсивно идут в случае использования поташа. [15]
Страницы: 1 2 3 4