Гидротриоксид
Cтраница 1
Гидротриоксиды являются типичными пероксидны-ми соединениями. Повышение температуры обусловливает относительный рост доли радикальных процессов, характеризующихся более высокими значениями энергий активации и предэкспоненциальных множителей. При низких температурах более вероятны процессы полярной перегруппировки без образования радикальных интермедиатов. [1]
Гидротриоксиды декалина, адамантана, 1 3 - и 1 4-диметилциклогексана и изо-пентана синтезируют методом сухого озонирования. Субстрат ( 1 - 3 ммоль), растворенный в пентане, приливают к свежепрокаленному адсорбенту ( 6 г) при интенсивном перемешивании. Растворитель выпаривают в роторном испарителе при комнатной температуре в вакууме водоструйного насоса. Адсорбцию изопентана проводят в запаянной ампуле при нагревании. С и выдерживают 1 - 3 ч при той же температуре. Количество поглощенного озона определяют спектрофотометрически. Непрореагировавший озон выдувают током кислорода. Из-за высокой адсорбирующей способности силикагеля при низких температурах не удается полностью извлечь гидротриоксиды, поэтому выход ROOOH не превышает - 30 - 60 % в расчете на исходный субстрат. [2]
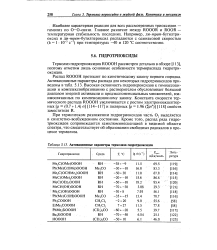 |
Активационные параметры термолиза гидротриоксидов. [3] |
Термолиз гидротриоксидов ROOOH рассмотрен детально в обзоре [113], поэтому отметим лишь основные особенности термораспада гидротриоксидов. [4]
Этим методом получены гидротриоксиды неактивированных углеводородов ( 2-метилбутан, 1 3 - и 1 4-диметилцик-логексаны, адамантан и др.), которые не образуются в условиях жид-кофазного озонирования. Высокополярная поверхность силикагеля стабилизирует ионные интермедиаты озонирования, что благоприятствует образованию ROOOH даже в случае неактивированных углеводородов. [5]
Для получения: гидротриоксидов МеСН ( ОН) ОООН, EtCH ( OH) OOOH, Ме2С ( ОН) ОООН, Et ( Me) C ( OH) OOOH, зо - РЮСМе2ОООН, MeC ( OEt) 2OOOH, МеСОСН ( ОООН) Ме, МеСОСН ( ОООН) Рг, Х - С6Н4С ( О) ОООН ( X и - МеО, о - С1, л - С1, л - С1, o - F) проводят озонирование этанола, пропанола-1, пропанола-2, бутаНо - ла-2, диизопропилового эфира, 1 1-диэтоксиэтана, метилэтилкетона, метилбутил-кетона, бензальдегида и его производных соответственно в реакторе объемом 10 мл в течение 20 - 120 мин. Скорость подачи озон-кислородной смеси 100 мл / мин ( 2 % О3), объем озонируемого образца 2 - 3 мл. При получении гидротриоксидов спиртов, 1 1-диэтоксиэтана, диизопропилового эфира и кетонов озонирование проводят в среде субстрата окисления. Синтез гидротриоксидов спиртов и 1 1-диэтоксиэтана проводят при - 80 н - - 40 С, в остальных случаях температуру варьировали в пределах - 80 - н - 20 С. Полученные таким образом гидротриоксиды продувают аргоном и хранят в темноте при - 80 С. Выход ROOOH в расчете на израсходованный RH зависит от строения субстрата и достигает 70 - 90 % для гидротриоксидов спиртов. [6]
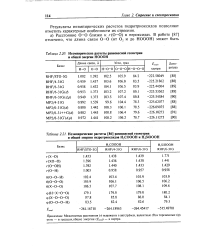 |
Неэмпирические расчеты равновесной геометрии и общей энергии НОООН.| Неэмпирические расчеты равновесной геометрии. [7] |
Результаты неэмпирических расчетов гидротриоксидов позволяют отметить характерные особенности их строения. [8]
При термическом разложении гидротриоксидов часть О2 выделяется в синглетно-возбужденном состоянии. Кроме того, распад ряда гидротриоксидов сопровождается хемилюминесценцией в видимой области спектра, что свидетельствует об образовании свободных радикалов в процессе термолиза. [9]
К настоящему моменту синтезированы гидротриоксиды ROOOH спиртов, простых эфиров, ацеталей, альдегидов и кетонов. [10]
Первое направление реализуется для гидротриоксидов силанов. Кинетические и активационные параметры распада ( высокое отрицательное значение энтропии активации), значительный эффект заместителя, зависимость скорости распада от полярности растворителя, а также отсутствие влияния радикального ингибитора ионола на кинетику распада согласуются с преимущественно молекулярным ( 90 %) механизмом разложения. [11]
Торсионный угол ф в гидротриоксидах характеризует положение атомов-заместителей относительно плоскости, образуемой тремя атомами кислорода. Найдено, что триоксид водорода существует в двух устойчивых конформациях, различающихся положением атомов Н относительно триоксидной плоскости. [12]
При температуре выше О С гидротриоксиды рачлагаются с образованием монозфиров гликолей, однако эта реакция менее селективная. [13]
Несмотря на то, что в гидротриоксидах спиртов, эфиров, ацеталей возможно образование внутримолекулярной водородной связи ( это позволило [ 126] предположить для них молекулярный путь распада - [ реакция ( I) ]), совокупность экспериментальных данных в целом лучше согласуется с радикальным механизмом расщепления ROOOH, показанным на примере гидротриоксида этанола. [14]
К ним относятся триоксид водорода НОООН, органические гидротриоксиды ROOOH, триоксиды алкилов и аралкилов ROOOR. Первичные озониды ( 1 2 3-триоксоланы, Е) и трансаннулярные озониды ( F) можно рассматривать как циклические аналоги триоксидов. [15]
Страницы: 1 2