Гидрофосфат - калий
Cтраница 1
Гидрофосфат калия как соль диссоциирует полностью К2НРО4 - 2К НРОГ. [1]
Имеются вода и гидрофосфат калия. Выберите только одно основание и одну кислоту и получите с использованием четырех веществ, а также продуктов их взаимодействия следующие вещества: фосфат бария, гидрофосфат бария, нитрат бария, гидроксид калия, дигидрофосфат калия. [2]
Растворяют 5 г гидрофосфата калия ( К2НР04) в 50 мл воды. Доводят рН раствора до 9 добавлением 27 % - ного раствора едкого натра и разбавляют водой до 100 мл. [3]
Для целей управления лазерным излучением первыми начали применяться кристаллы гидрофосфата калия KH2P04 ( KDP) и аналоги на его основе, в которых калий замещается группой аммония, а водород - тяжелым изотопом - дейтерием. Кристаллы типа KDP выращиваются из водных растворов, технология их выращивания достигла высокого уровня и продолжает совершенствоваться. Получаемые кристаллы KDP высокого оптического качества до настоящего времени находят широкое применение. [4]
Растворяют 16 73 г гидрофосфата дикалия Р и 0 52 г гидрофосфата калия Р в воде до получения 1000 мл. Стерилизуют раствор в течение 20 мин в автоклаве при 120 С и, если необходимо, доводят рН до 7 9 - 8 1 фосфорной кислотой ( - 1440 г / л) ИР или раствором гидроокиси калия ( - 110 г / л) ИР. [5]
Из 8 4 г едкого кали 6 72 г расходуются на превращение фосфорной кислоты в гидрофосфат калия, а 1 68 г ( 8 4 - 6 72 1 68) - на превращение гидрофосфата калия в фосфат. [6]
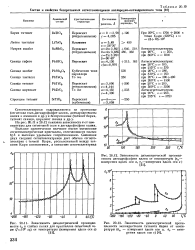
На рис. 20.11 и 20.12 показана зависимость е от температуры для сегнетовои соли и ди гидрофосфата калия. [8]
Cu ( NO3) 2 на колонках желатина, содержащего 1 5 % - ный раствор гидрофосфата калия, получаются две полосы: верхняя, светло-желтая, содержит фосфат железа ( III), нижняя, голубая, содержит гидрофосфат меди ( II), Полосы разделены большим промежутком прозрачного геля. [9]
Методом осадочной хроматографии в геле желатины нам удалось провести разделения солей железа, кобальта, никеля и меди, путем применения различных осадителей: гидрофосфата калия, железистосинеродистого калия, диметилглиоксима, 8-оксихинолина. [10]
Кларка и Лаб-са для интервала рН 2 - 10, которые получают, используя три системы: фталевая кислота - бифталат калия, дигидрофосфат калия - гидрофосфат калия и борная кислота - борат натрия. [11]
Из 8 4 г едкого кали 6 72 г расходуются на превращение фосфорной кислоты в гидрофосфат калия, а 1 68 г ( 8 4 - 6 72 1 68) - на превращение гидрофосфата калия в фосфат. [12]
Из приведенных выше уравнений видно, что для превращения 0 06 г-моль фосфорной кислоты в дигидрофосфат калия необходимо 0 06 г-моль едкого кали, для превращения 0 06 г-моль фосфорной кислоты в 0 06 г-моль гидрофосфата калия необходимо 0 12 г-моль едкого кали, а для превращения 0 06 г-моль гидрофосфата калия в 0 06 г-моль фосфата калия нужно еще 0 06 г-моль едкого кали. Таким образом, из 0 15 г-моль едкого кали 0 12 г-моль его расходуется на образование 0 06 г-моль гидрофосфата калия, а 0 03 г-моль ( 0 15 - 0 12 0 03) едкого кали расходуется на превращение 0 03 г-моль гидрофосфата в 0 03 г-моль фосфата калия. Значит, после выпаривания раствора в остатке будут 0 03 г-моль, или 0 03 212 6 36 г, фосфата калия и 0 03 г-моль ( 0 06 - 0 03 0 03), или 0 03 174 5 22 г, гидрофосфата калия. [13]
В соответствии с двумя номенклатурами кислые соли называют следующим образом: NaHSO4 - кислый сернокислый натрий, или гидросульфат натрия; КН2РО4 - однозамещенный фосфорнокислый калий, или дигидро-фосфат калия; К НРСХ - двузамещенный фосфорнокислый калий, или гидрофосфат калия; Са ( НСО3) 2 - кислый углекислый кальций, или гидрокарбонат кальция. [14]
В соответствии с двумя номенклатурами кислые соли называют следующим образом: NaHSO4 - кислый сернокислый натрий, или гидросульфат натрия; КН2РО4 - однозамещенный фосфорнокислый калий, или дигидро-фосфат калия; К2НРО4 - двузамещенный фосфорнокис лый калий, или гидрофосфат калия; Са ( НСОз) 2 - кислый углекислый кальций, или гидрокарбонат кальция. [15]
Страницы: 1 2 3