Гильдебранда
Cтраница 1
Гильдебранда выдвинула деление всего хозяйств, развития на три стадии: натуральное, денежное и кредитное х-во. К тому же в схеме отсутствует разделение на простое товарное и капиталистич. Вместе с тем дон. [1]
Гильдебранда связаны с обоснованием закономерностей идеальных растворов. [2]
Гильдебранда ( 5), являющийся функцией энергии когезии: S VE / V, где Е - молярная энергия когезии, оцениваемая для растворителя по энергии испарения; V - мольный объем растворителя. Параметр растворимости 8 растворителя должен быть близок к параметру растворимости полимера, но последнюю величину рассчитать точно довольно трудно. Второй характеристикой служит способность растворителя к образованию водородных связей ( Дц), которую определяют с помощью ИК-спектроскопии. [3]
Гильдебранда для растворителя и полимера соответственно ( параметр растворимости Гильдебранда равен по величине квадратному корню из энергии испарения единицы объема жидкости 8 V& EKcn. [4]
Гильдебранда выполняется лучше, чем правило Трутона. [5]
Гильдебранда связаны с обоснованием закономерностей идеальных растворов. [6]
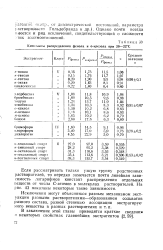 |
Константы распределения фенола и о-крезола при 20 - 22 С. [7] |
Гильдебранда и др.) - Однако почти всегда имеется и ряд исключений, свидетельствующий о сложности: - тих взаимоотношений. [8]
Гильдебранда при 25 С; So - растворимость экстрагента в воде при 20 С; SB-растворимость воды в экстрагенте при 20 С. [9]
Гильдебранда, в основу которой положена полярность растворителя, характеризуемая отношением энергии поляризации применяемого растворителя к энергии поляризации н-пентана, принятой за нуль. [10]
Согласно Гильдебранду [70], отклонение реальных растворов от закона Рауля пропорционально разности квадратных корней из плотностей энергий растворенного вещества и растворителя. Позже, пользуясь несколько более общим методом, к тому же заключению пришел Скэтчард [71], уравнения которого мы здесь выводим, прибегая к тем же обозначениям, что и при нашем изложении теории Ван-Лаара. [11]
Согласно Гильдебранду, зависимость величины Al / исп от температуры и объема жидкости ( последний ся при изменении температуры и внешнего давления) можно вить функцией вида a ( T) / Vn, причем для многих веществ значение п близко к единице. [12]
По Гильдебранду основная причина отклонения реальных растворов от поведения регулярных растворов - притяжение одинаковых или разнородных молекул друг к другу, обусловленное их полярностью. За счет взаимного притяжения молекул полярного компонента может происходить выталкивание молекул другого - неполярного компонента. Результатом этого является положительное отклонение от закона Рауля. При большой разнице полярностей компонентов может иметь место их ограниченная взаимная растворимость. Большее притяжение между разнородными, чем между однородными молекулами, обусловливает отрицательные отклонения от идеального поведения. [13]
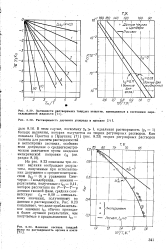 |
Влияние состава твердой фазы на растворимость аргона в азоте. [14] |
Скэт-чарда - Гильдебранда, нижняя - результаты, полученные с / 12 - 0 11, которое рассчитано по Я-У - Т - у данным газовой фазы, средняя соответствует / 1Й 0 08 - оптимальному значению, полученному по данным о растворимости. [15]
Страницы: 1 2 3