Гиршфельдер
Cтраница 3
Для расчета плвтности в однофазной области за основу было взято термическое уравнение состояния Гиршфельдера [6, 16, 17], которое было модифицировано и приведено к форме, не требующей для своего использования рс, Zc и ас. Следует отметить, что при этом Zc и ас теряют свой первоначальный смысл и превращаются в подгоночные параметры, которые используются для расчета ряда констант уравнения состояния и комплекса приведения по плотности для наилучшего описания уравнением состояния Р - V - Т свойств газов и жидкостей. [31]
Величина Х3 характеризует теплопроводность нереагирующей смеси и может быть рассчитана как по формуле Гиршфельдера ( 4 - 29), так и по другим формулам. [32]
Достаточно точным методом расчета мольного объема вещества в паровой фазе является также метод Гиршфельдера, Бюлера, Мак-Ги и Саттона. Этот метод, как и метод Редлиха-Квонга, также требует компьютерных расчетов в связи с нелинейностью основных уравнений, которые имеют разный вид для двух различных областей параметров газа в приведенном виде. [33]
Мэсон и Саксена [88] упростили точное выражение для k одно атомных веществ и, использовав предложение Гиршфельдера об определении коэффициента Эикена для смеси, нашли, что значение Aij в уравнении ( IX. [34]
Molecular Theory of Gases and Liquids, Wiley, New York, 1964; имеется русский перевод первого издания: Гиршфельдер Дж. [35]
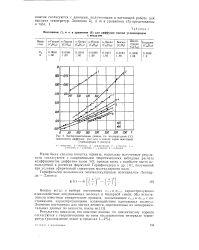 |
Экспериментальные данные по температурной ( С. [36] |
Нами была сделана попытка оценить, насколько полученные результаты согласуются с современными теоретическими методами расчета коэффициентов диффузии газов [10], прежде всего с наиболее часто используемой в расчетах формулой Гиршфельдера и др. [11], полученной при условии сферической симметрии молекулярного поля. [37]
Оценка-погрешности вычисления ДЯр, г с использованием уравнений состояния Бенедикта - Вебба - Рубина, Редлиха - Квонга в модификации Барсука, Зудкевича, Ли - Эдмистера, Ямада, Гиршфельдера с соавторами проводилась на примере небольшого числа веществ и смесей в газообразном состоянии и составляет 4 - 10 кДж / кг. Расчет приращения парциальной энтальпии с применением уравнений состояния БВР и РК также рекомендуется проводить лишь для газовых смесей. [38]
Значения коэффициентов переноса для различных моделей молекул как в первом, так и в более высоких приближениях для чистого газа и газовых смесей можно найти в неоднократно уже цитированных монографиях Чспмона и Каулинга и Гиршфельдера, Кертиса и Берда. [39]
Таблицы функций В ( Т) и С ( Т) и их производных, а также функций В ( Т, t) и С ( Т, t) приведены в кн.: Гиршфельдер Дж. [40]
Этот факт вносит дополнительную неопределенность. Гиршфельдер, Кертисс и Берд [75] дали простую ( и ебольшую по объему) таблицу z0 / k и о, в которой отдельно приводятся значения, полученные по данным о вязкости и по Р - V - Т данным. [41]
Уравнение (11.35) представлено графически на рис. II. Гиршфельдер, Кертисс и Берд [33] рассчитали также третий ви-риальный коэффициент с помощью сложной процедуры численного интегрирования. [42]
Использовать при проведении технических расчетов точные методы, основанные на принципах статистической механики, очень трудно. Поэтому Гиршфельдер и его сотрудники предложили ввести в уравнения для определения физико-химических постоянных вещества функции от а и е, значения которых они рассчитали и свели в таблицы ( см., например, табл. IV-5), исключив тем самым необходимость частого выполнения сложных вычислений. [43]
Использовать при проведении технических расчетов точные методы, основанные на принципах статистической механики, очень трудно. Поэтому Гиршфельдер и его сотрудники предложили ввести в уравнения для определения фи-зико-хпмических постоянных вещества функции от а и е, значения которых они рассчитали и свели в таблицы ( см., например, табл. IV-5), исключив тем самым необходимость частого выполнения сложных вычислений. [44]
Это уравнение подобно уравнению Ван-дер - Ваальса, за исключением того, что в ( VI. Как отметил Гиршфельдер, уравнение Эйринга можно рассматривать как предельную форму уравнения Ван-дер - Ваальса, которая получается для случая перекрытия твердых сфер. В [596] на примерах нескольких жидкостей показано, что значения сжимаемости и коэффициента термического расширения, вычисленные по уравнению Эйринга, удовлетворительно согласуются с экспериментальными данными. [45]
Страницы: 1 2 3 4