Гликозидирование
Cтраница 1
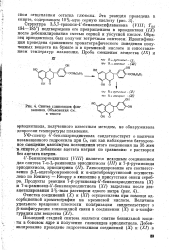 |
Синтез глико идов фла. [1] |
Гликозидирование его соответственно J-L - ацетобрОмрамнозой и а-ацетобромрутинозой осуществлено по Кенигсу - Кнорру в хинолине в присутствии окиси серебра. [2]
Гликозидирование увеличивает растворимость А. [3]
Гликозидирование обусловливает понижение величины Rf. Введение одного остатка глюкозы вызывает эффект приблизительно такой же, как и введение одной гидроксильной группы. [4]
Гликозидирование антоцианидинов сопровождается гипсохромным сдвигом максимума поглощения. Природные антоцианины всегда являются 3 - или 5-моногликозидами или 3 5-дигликозидами антоцианидинов. Хар-борн / 89 / опубликовал данные для пятидесяти природных антоцианинов и антоцианидинов. [5]
Гликозидирование простейших фенольных соединений осуществляется двумя ферментными системами: гликозилтрансферазной и р-глюкозидазной. [6]
Процесс гликозидирования флавонолов, подобно процессу галлирования катехинов, по-видимому, пространственно разобщен в клетке от процессов биосжнтеза агликонов. [7]
МНз-группы, которая отталкивает протон, катализирующий реакцию гликозидирования ( см. стр. Поэтому для получения гликозидов 2-амино - 2-дезоксиса-харов, которые обычно носят название гликозаминидов, применяют обходные пути. Так, например, проводят замещение аминогруппы группировкой, устойчивой к кислотам, которую после гликозидирования можно удалить в нейтральной или щелочной среде. Обычно для этой цели используется введение карбалкоксильной 19 или 2 4-динитрофенильной 20 группировок. Для получения гликозидов 2-амино - 2-дезоксисахаров можно использовать меркаптали их аль-форм, которые при расщеплении бромом 21 или сулемой 22 в абсолютном спирте гладко превращаются в гли-козиды. Использование для синтеза гликозаминидов реакции Кенигса - Кнорра, которая является общим методом синтеза гликозидов ( см. гл. Так, например, бромгидрат 3 4 6-три - О-аце-тил - а - О-глюкозаминилбромида, который образуется при действии бромистого ацетила на Д - глюкозамин 23, нерастворим в растворителях, применяемых в реакции Кенигса - Кнорра, и поэтому пригоден только для получения гликозаминидов низших спиртов. Если соли гликозаминилгалогенидов и галоидоводородных кислот представляют устойчивые соединения, то их N-ацильные аналоги очень неустойчивы и должны использоваться сразу после приготовления. [8]
Последующие процессы метилирования ( Finkle, Nelson, 1963), гликозидирования ( Hutchinson, Roy, Towers, 1958; Pridham, 1958; Friedrich, 1960; Barber, 1962; Ямаха, 1962) и гидроксилирования ( Ibrahim, Towers, 1959; Mason, Onopryenko, Buhler, 1957; Buhler, Mason, 1961; Winicki, Chopin, Cier, 1960; Thomas, Loughman, Powell, 1963; Hanson, Zucker, 1963) фенольных соединений широко распространены в высших растениях и носят вторичный характер. [9]
Дальнейшие, более тонкие различия в спектрах зависят от положения заместителей, образующихся при метилировании, ацетили-ровании или гликозидировании. [10]
 |
Биологическая активность кверцетин-гликозида ( квер-цитрина ( /, КГК ( 2 п-кумаровой кислоты ( 3 ( Чумаковскийг Кефели, 1968. [11] |
Снижение активности n - кумаровой кислоты в молекуле КГК может быть связано не только с увеличением общего молекулярного веса КГК, но и с рядом других факторов, к которым могут быть отнесены: а) гликозидирование молекул n - кумаровой кислоты, б) ослабление ее проникающей способности в результате связывания с кверцетин-гликозидом. [12]
Хотя и общепризнано, что разложение флавонолов в щелочной среде протекает медленно, Джерд и Горовиц / 83 / показали, что стабильными в растворе этилата натрия являются те флавонолы, у которых гидроксил в положении 3 защищен метилированием или гликозидированием. На стабильность не оказывают влияния ни число, ни положение прочих гидроксильных групп, хотя исключения из этого правила обнаруживаются, если присутствует пирогаллольная группировка. [13]
Гидролизом 0, 4 % - ной соляной кислотой в ацетоне из пен-таацетилкверцетина был получен 3, 5, 7, 31-тетраацетил - 41-оксифлавон. Гликозидированием этого соединения бромацетилглюкозой в ацетоне в присутствии окиси кальция и небольшого количества щелочи получен 3, 5, 7, 31-тетраацетил - 41-ацетилглюкозид кверцетина. Из продуктов щелочного гидролиза ацетата глюкозида изолирован кверцетин - - 41 - О - - Р - D-глюкопиранозид. Гидролизом в безводной среде 0, 005 н раствором метилата натрия пентаацетилкверцетина был получен 3, 5, 7-три-ацетилкверцетин. В результате реакции этого соединения и бро-мацетилглюкозы в присутствии окиси кальция и окиси серебра синтезирован кверцетин-31, 41 - О - р - О-диглкжопиранозид. [14]
Для избирательного метилирования и гликозидирования проведена предварительная защита ацетилиро-ванием некоторых производных 2-фенилбензо-у - пирона с последующим избирательным гидролизом ацетильных групп в местах, подлежащих замещению. Избирательное метилирование проводилось также и без предварительного ацетилирования реакцией с диметилсульфатом в присутствии некоторых комплексообразующих реагентов, в частности, буры. Для избирательного метилирования положений 3, 4 вначале были получены ацетаты веществ кверцетина и рутина, которые затем подвергались щелочному гидролизу 0 0025 N раствором метилата натрия, что позволило дезацетилировать упомянутые выше соединения по положениям 3 4 и получить 3 4 -диме-тилкверцетин ( t 155 - 160 С, А, 370, 256 нм) и 3 4 -диметилрутин ( tni160 - 165 C, Xmax 352, 255 нм) после метилирования диметилсульфатом в ацетоне с последующим омылением образовавшихся метилированных ацетатов. [15]
Страницы: 1 2