Глюкоамилаза
Cтраница 1
Глюкоамилаза ( 1 4-а - О-глюкан глюкогидролаза или экзо-1 4-а-глюкозидаза, КФ 3.2.1.3) из Rhlzopus delemar. [1]
Высокоочищенная глюкоамилаза получилась после фракционного осаждения этанолом и последующего отделения транс-гликозилазы на ДЭАЭ-целлюлозе. После диализа проводится высаливание сернокислым аммонием, затем снова диализ и осаждение ферментов ацетоном. [2]
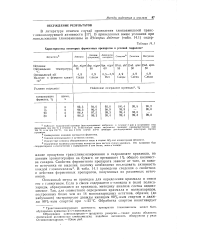 |
Характеристика некоторых ферментных препаратов и условий гидролиза3. [3] |
Трансгликозилирующая активность препаратов глюкоамилазы может быть обусловлена примесью a - D-глюкозидазы. [4]
По их данным, глюкоамилаза в зависимости от длины цепи расшеп-ляет глюкозидные связи различными способами. [5]
Затем, продолжая гидролиз с помощью глюкоамилазы 3Н 4 - 5 6, температура 55 - 60 С), получают D-глюкозу, кото-о изомеризуют с помощью фермента глюкозоизомеразы эН 6 - 6 2, температура 60 - 70 С) во фруктозу. Получают глю -) 3о - фруктозные сиропы с содержанием 45 - 50 % фруктозы и - 60 % глюкозы. Они имеют такую же сладость, как и сахара. [6]
Гидролиз крахмала катализируют а-амилаза, р-амилаза и глюкоамилаза. Эти ферменты различаются по своим свойствам, способу воздействия на крахмал и распространению в природе. Кроме того, - амилаза различного происхождения имеет существенные отличия в свойствах и механизме действия на крахмал. [7]
Глубинная культура Глюкаваморин Гх-466, являющаяся высокоактивным источником глюкоамилазы, может применяться для оса-харнвання в смеси с Амнлорнзнном Пх или Амнломезентерином Гх, служащими нсточннкамн - амилазы. [8]
Наиболее широко выпускаются следующие типы препаратов: бактериальная и грибная амилазы, глюкоамилаза, бактериальная и грибная протеазы, целлюлаза, липаза, пектиназа. Во многих случаях вырабатываются и используются комплексы различных ферментов. Препараты часто имеют технические ( фирменные) названия. [9]
В последнее время на спиртовых заводах СССР стал широко применяться высокоактивный по глюкоамилазе штамм Asp. В связи с этим эту культуру целесообразно применять в смеси с другими культурами, продуцирующими а-амилазу и протеолитические ферменты. [10]
Метод основан на определении количества глюкозы, образующегося при гидролизе растворимого крахмала ферментом глюкоамилазой. [11]
Из этой таблицы видно, что при осахаривании культурами плесневых грибов, богатых глюкоамилазой, конечным продуктом гидролиза является не мальтоза, а глюкоза. Очевидно, при добра-живании скорость гидролиза конечных декстринов плесневыми грибами будет опережать скорость гидролиза ферментами зернового солода, в результате чего сусло независимо от образования Сахаров в первой стадии гидролиза сбродится быстрее. Продолжительность гидролиза в пер вой стадии не имеет большого значения, и в ней можно ограничиться только охлаждением и смешиванием разваренной массы с культурами плесневых грибов. [12]
Методы рснованы на специфическом определении глюкозы, образующейся при гидролизе растворимого картофельного крахмала и продуцируемой ферментом глюкоамилазой. [13]
Некоторые поли-о-глюкозы, являющиеся продуктами деградации ( декстринизации, термической обработки) крахмала, не гидролизуются глюкоамилазой. Описанный метод позволяет определить содержание только тех продуктов, которые подвержены действию этого фермента. Определив общее количество гексоз ( например, антроновым методом), по разности результатов этих двух анализов можно найти содержание в образце нормального и модифицированного крахмала. [14]
В группе карбогидраз можно отметить две подгруппы, которые находят широкое применение: а) амилазы и амилоглюкозидаза ( глюкоамилаза), гидролизующие крахмал; б) ферменты, расщепляющие низкомолекулярные углеводы - мальтаза, лактаза, сахараза и др. Используются амилазы: животная ( из поджелудочной железы), растительная ( из проросших зерен злаков), а также бактерий и микроскопических грибов. Все они отличаются между собой рядом важных свойств. [15]
Страницы: 1 2 3