Группа - молекула
Cтраница 1
Группы молекул или ионов в жидкой или газовой фазах, связанные водородными связями, ван-дер-ваальсовыми или электростатическими взаимодействиями. [1]
Группы молекул соединены в структуры более высокого порядка, видимые в электронном микроскопе и называемые фибриллами. [2]
 |
Влияние степени дисперсности на точку плавления салола. [3] |
Группа молекул, связанных друг с другом, образует систему, в которой существует микроскопическая поверхность и которая обладает определенным поверхностным натяжением, поверхностной энергией. Влияние поверхностной энергии на физические и химические свойства вещества можно очень ясно наблюдать на следующих примерах. Из физики известно, что упругость пара жидкости зависит от кривизны ее поверхности. [4]
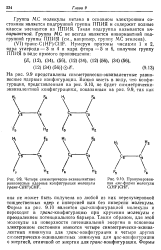 |
Четыре симметрически-эквивалентные равновесные ядерные конфигурации молекулы гранс - С ( НР СНР.| Пронумерованная ijuc - форма молекулы C ( HF CHF. [5] |
Группа МС молекулы метана в основном электронном состоянии является подгруппой группы ППИЯ и содержит полные классы элементов из ППИЯ. Такая подгруппа называется инвариантной. [6]
Группа СЮз молекулы хлорной кислоты представляет собой правильную тригональную пирамиду с атомом хлора в вершине. Длина связей С1 - О составляет 1 42 0 01 А. [7]
Группой МС молекулы N02 является группа C2v ( M), приведенная в табл. А. [8]
Вторая группа молекул вызывает ослабление интенсивности и уширение полосы поглощения поверхностных гидроксильных групп со значительно большим смещением, достигающим 300 см. - 1, В эту группу входят молекулы, взаимодействующие с гидроксильными группами за счет слабой водородной связи, такие, как. [9]
Переход группы молекул ( ионов) примеси в группу соседних узлов или междоузлий кристаллической решетки. [10]
Прототипом этой группы молекул может служить карбонил никеля. [11]
Полярные же группы молекул дозируемого вещества при адсорбции на неполярном адсорбенте из полярного элюента уменьшают удерживание, так как их межмолекулярное взаимодействие с полярными группами молекул элюента, влияя на их ориентацию, ослабляет межмолекулярное взаимодействие молекул дозируемого вещества с адсорбентом и облегчает их возвращение в объем элюента. Таким образом, в этом случае удерживание в основном определяется, во-первых, неспецифическим межмолекулярным взаимодействием молекул дозируемого вещества с адсорбентом и, во-вторых, специфическим межмолекулярным взаимодействием этих молекул с элюентом, причем последнее уменьшает удерживание. Этот молекулярный механизм удерживания надо иметь ввиду, так как распространенный в литературе по жидкостной хроматографии термин обращеннофазная хроматография не передает существа дела. Действительно, из лекции 16 следует, что органические вещества, во-первых, удерживаются из водных растворов и на полярном адсорбенте ( гидроксилированной поверхности силикагеля) и, во-вторых, порядок выхода органических веществ может быть изменен при изменении состава элюента как на полярном, так и неполярном адсорбентах. [12]
Квантовая механика группы молекул ТЦХМ может быть упрощена путем учета симметрии индивидуальных молекул. Как уже установлено, интересующая нас молекулярная орбиталь принадлежит к представлению Вая каждой молекулы ТЦХМ, а 2Рг - орбитали расположены так, что имеется В2й - симметрия. [13]
К этой группе молекул следует отнести также и молекулы насыщенных углеводородов, где между атомами углерода имеются только а-связи. [14]
При разделении на группы молекул подобная оценка может оказаться весьма полезной, что более подробно будет рассмотрено в разд. [15]
Страницы: 1 2 3 4