Хорошо уходящая группа
Cтраница 1
Хорошо уходящие группы в положениях 2, 4 и 6 пиримидина достаточно легко замещаются нуклеофилами ( разд. Хлоропроизводные пиримидина могут быть получены при взаимодействии соответствующих пиримидинонов с оксихлоридом фосфора ( аналогично превращению пиридона-2 в 2-хлоропиридин; см. гл. Хлор легко замещается при действии таких нуклео-филов, как амины, алкоксид-ионы, тиолы и гидразин. Это позволяет провести селективное замещение в 2 4-дихлоропроизводном только одного атома галогена. Кроме галогена, в некоторых случаях возможно нуклеофильное замещение метилсульфонильной группы. Даже метоксигруппу можно заместить более сильным нуклеофилом; например, при действии на 4-метоксипиримидинон - 2 аммиака образуется цитозин. [1]
Нуклеофильное замещение хорошо уходящей группы, обычно атома галогена, имеет очень важное значение в химии гетероциклических соединений, особенно для получения различных производных шестичленных электронодефицит-ных гетероциклических соединений. Реакции нуклеофильного замещения возможны также в азолах в том случае, если уходящая группа присоединена к иминному фрагменту. [2]
Аминогруппы превращаются в хорошо уходящие группы модификацией их в 1 3 4-триазол. [3]
В присутствии относительно хорошо уходящих групп, таких как феноляты или кислые спирты ( например, трифторэтанол), медленной стадией является отрыв от днполярного тетраэдрического иптермедиата кислородной уходящей группы. [4]
Однако при наличии хорошо уходящей группы ( 121, R2 Аг) вступает в силу альтернативный механизм. Образующийся промежуточный изоцианат может быть захвачен нуклеофилом, находящимся в растворе, и далее может превратиться в продукт замещения. [5]
Сульфонилоксигруппы или любые другие хорошо уходящие группы, соответствующим образом расположенные в молекуле моносахарида, подвергаются бимолекулярному нуклеофильному замещению ( 5N2) кислородсодержащими нуклеофилами, такими как бензоат или ацетат, в биполярных апротонных растворителях ( например, в / У. Реакционная способность при таком замещении по механизму 5N2 зависит от природы моносахарида и места замещения. Ричардсон [43] сформулировал правило, основанное на стерео-электронных факторах в переходном состоянии, с помощью которых можно предсказать относительную реакционную способность сульфонилоксигрупп, присоединенных к пиранозному циклу. [6]
 |
Зависимость легкости гидроксилирования гетероциклов с помощью КОН от величины положительного л-заряда на а-углеродном атоме q a [ 4Q7, 418 ]. [7] |
Энергетический профиль реакций замещения таких хорошо уходящих групп, как Cl, SO2Me, NOa, должен также соответствовать типу кривой / ( на рис. 7.1), поэтому и здесь можно ожидать корреляции между величиной я-заряда и легкостью превращения. Анализ большого количества кинетических данных показывает, что эти надежды оправдываются частично. [8]
Когда сложный эфир содержит очень хорошо уходящую группу, как в случае 2 4-динитрофе-нилацетата, метод слежения по анилину показывает, что реакция идет по механизму нуклеофильного катализа, ибо количество образующегося ацетанилида достаточно для такого вывода. В другом случае, как мы видели, ацетат не влияет на скорость гидролиза этилацетата. В этом случае уходящая группа, этоксид-ион, гораздо хуже ацетата, и нуклеофильный катализ не имеет места. [9]
С другой стороны, при замещении хорошо уходящих групп скорость реакции определяется первой стадией. Соответствующие о-ком-плексы чрезвычайно неустойчивы. Так, до сих пор нет примеров достоверной регистрации о-комплексов, в геминальном узле которых одновременно находились бы галоген и замещающий его нуклеофил. [10]
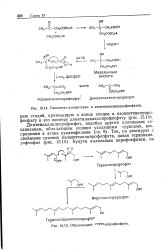 |
Биосинтез изопентенил - и диметилаллилпирофосфатов.| Образование геран. ЛПИр0фосфата. [11] |
Диметилаллилпирофосфат, подобно другим аллильным соединениям, обладающим хорошо уходящими группами, восприимчив к атаке нуклеофилами ( гл. [12]
 |
Кинетические данные реакций ( 30 и ( 31. [13] |
Традиционное объяснение указанных несоответствий заключается в том, что структура переходного состояния при замещении хорошо уходящих групп лежит значительно ближе к а-ком-ттлексу, чем к исходной молекуле, в силу чего скорость процесса контролируется не столько величиной атомного заряда, сколько стабильностью а-комплекса. Это объяснение, однако, вряд ли удовлетворительно. Во-первых, энергии локализации недостаточно хорошо коррелируют с относительной активностью указанных соединений. [14]
Многие реакции процессов метаболизма довольно сложны, однако они похожи на реакции, рассмотренные в предыдущих главах. Например, фосфорилирование гидроксильных групп превращает их в хорошо уходящие группы, и - поэтому соседний атом углерода становится восприимчивым к нуклеофильной атаке ( гл. [15]
Страницы: 1 2