Первая группа - реакция
Cтраница 2
Первая группа реакций является простейшим случаем мехмолекулярного взаимодействия карбенов и их аналогов. При рекомбинации двух секстетных частиц образуется димерная молекула, содержащая кратную SI-связь. При взаимодействии большего числа частиц могут получаться полимеры линейного или циклического строения. Механизм димериза-иии синглетных и тришетных частиц различен. Квантово-химический расчет расширенным методом йзккеля [31] показал, что для двух синглетных метиле-нов сближение в одной плоскости по пути наименьшего движения имеет большой барьер активации, появление которого связано с запретом по симметрии. [16]
Для полисульфидных олигомеров, содержащих до 40 % химически связанной серы, наиболее интересны два типа превращений: по концевым HS-группам и полисульфидным звеньям макромолекул. Первая группа реакций мало чем отличается от классических превращений низкомолекулярных меркаптанов. Применительно к полисульфидным олигомерам такие макро-молекулярные реакции используются в процессах отверждения и химической модификации ( они рассмотрены в гл. Обменные и деструктивные реакции с участием полисульфидных групп протекают как при синтезе и хранении олигомеров, так и в специально проводимых деструктивных процессах, когда требуется понизить молекулярную массу полимера. [17]
Если не считать процесса сульфирования остаточного количества тиофена, вторая группа реакций является нежелательной, приводящей к образованию кислой смолки, ухудшению качества и уменьшению выхода регенерированной кислоты и дополнительным потерям бензольных углеводородов. Первая группа реакций является в основном полезной и необходимой для успешного проведения процесса, так как обеспечивает возможность получения бензольных углеводородов, в достаточной степени свободных от примесей тиофенов и непредельных соединений. Нежелательными в этой группе реакций являются процессы сополимеризации непредельных соединений и бензольных углеводородов, приводящие к уменьшению выхода последних и соответственно к увеличению выхода кубовых остатков. [18]
Химические способы получения оксидов хлора состоят в окислении соединений хлора низшей валентности или восстановлении хлора высшей валентности. Первую группу реакций используют обычно для маломасштабного или лабораторного получения оксидов. [19]
Преимуществом первой группы реакций является то, что их механизм, как правило, легче поддается изучению. Преимущество индикаторных реакций с участием органических реактивов заключается в возможности измерения их скорости фотометрическими методами ( светопоглощения, флуоресценции, хемилюминесценции) с высокой чувствительностью, особенно в хемилюминесцентных и флуоресцентных реакциях. [20]
Реакции окисления алкенов целесообразно подразделить на две большие группы: 1) реакции, в которых сохраняется углеродный скелет, 2) реакции окислительной деструкции углеродного скелета по двойной связи. К первой группе реакций относятся эпоксидирование, а также гидроксилирование, приводящее к образованию вицинальных транс - или г / ис-гликолей. Другая группа включает озонолиз и реакции исчерпывающего окисления алкенов, приводящие к образованию различного рода карбонильных соединений и карбоновых кислот. Мы последовательно рассмотрим обе эти важные группы реакций. [21]
Работа проводилась в двух направлениях: с одной стороны, была сделана попытка проведения некоторых реакций с использованием непосредственно самой фракции ( изготовлена на коксохимическом заводе Нижне-Тагиль - ского металлургического комбината), с другой стороны, изучались реакции с чистыми хинальдином и изохинолином с учетом того, что последние могут быть выделены из фракции. К первой группе реакций относятся реакции хинальдина с формальдегидом для получения таких мономеров как винилхинолин и хинолилпропандиол. Ко второй группе реакций относятся реакции хинальдина с различными диаминами для синтеза бис-тиохинальдинамидов - исходных продуктов для получения клешневидных полимеров и некоторые другие. [22]
В работе принято представление о кристалле как о растворителе, а реакции разделены на такие, которые могут изучаться независимо от установления внешнего равновесия, и такие, при которых требуется соблюдать равновесие с одной или более внешней фазой. К первой группе реакций относятся: ионизация самого кристалла, ионизация растворенного вещества, обмен между ионами и необратимые реакции, ведущие к агрегации. Ко второй группе относятся: установление равновесия в растворах внедрения, влияние отклонения от стехиометрии, а также реакции, в которых имеет место обмен между растворами замещения и растворами внедрения. [23]
Различают две большие группы каталитических реакций: гомогенный и гетерогенный катализ. В первой группе реакций катализатор и субстрат образуют одну фазу, обычно жидкую. Во второй группе реакций катализатор является твердым, а субстрат - жидким или газообразным. [24]
Природа внутрисферных лигандов как окисленной, так и восстановленной форм оказывает большое влияние на скорость и механизм переноса электронов между ними. При протекании первой группы реакций образуется продукт СгХ2, что доказывает внутрисферный механизм переноса электрона. [25]
Для алкинов характерны следующие три типа реакций: 1) присоединение; 2) восстановление и окисление; 3) замещение. В названии первой группы реакций нет разграничения на электрофильные, радикальные и нуклеофильные реакции присоединения, но будут приведены примеры каждой из этих реакций. Алкины - очень ценные и широко используемые вещества; ниже рассмотрены лишь самые обычные реакции присоединения, причем особое внимание обращается на те случаи, где существует отличие от химии алкенов. В последнем разделе рассматриваются те реакции, в которых замещается только кислый водород, и приведены некоторые примеры использования образующихся веществ. [26]
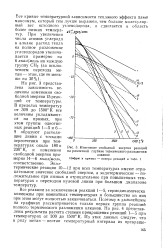 |
Изменение свободной энергии реакций на различной глубине термического разложения. [27] |
Все реакции за исключением реакций 1 - 5, термодинамически возможны при комнатных температурах и большинство из них при этом могут полностью заканчиваться. Поэтому в дальнейшем на графиках рассматривается только первая группа реакций полного термического разложения алканов. На рис. 4 представлены результаты расчета степени превращения реакций 1 - 5 при температурах от 300 до 1500 К. [28]
Температура пика-это такая температура образца, при которой завершилось данное превращение; в первой группе реакций эта температура является истинной температурой превращения. Во второй группе реакций истинную температуру превращения трудно определить, поэтому здесь обычно регистрируется та температура, при которой скорость реакции достаточно велика для отклонения кривой ДТА от нулевой линии. [29]
Были взяты группы с разной подготовкой: достаточно высококвалифицированные, средней квалификации, с недостаточной квалификацией. У первой группы реакции на неисправность нормализуются после ввода второго отказа действующей системы, а у лиц менее подготовленных - после 5 - 6 отказов. [30]
Страницы: 1 2 3