Аммониевая группа
Cтраница 3
Приведенные выше и ряд других экспериментальных данных аналогичного характера позволяют сделать общее предположение о том, что стабилизация аммониевой группой соседнего карбаниона осуществляется лишь за счет электростатического взаимодействия разноименных зарядов. В аммониевых соединениях у атома азота, являющегося элементом второго периода, заполнены все 2s - и 2 / 7-орбитали, а следующая свободная Ss-орбиталь имеет значительно более высокую энергию. В противоположность этому у атомов фосфора и серы, являющихся элементами третьего периода, в соединениях заполнены 3s - и Зр-орбитали, а следующие незанятые Зс ( - орбитали характеризуются энергией, лишь незначительно превышающей энергию Зр-орбиталей. [31]
Стабилизация может быть достигнута получением соли ( например, нитрованием в концентрированной серной кислоте), причем образуется ионизованная аммониевая группа, обладающая слабой мета-ориентацией. При стабилизации путем превращения в М - ацетиль-ное производное понижается легкость замещения в мета-положение и становится возможным получение орто - и пара-монопроизводных. [32]
Стабилизация может быть достигнута получением соли ( например, нитрованием в концентрированной серной кислоте), причем образуется ионизованная аммониевая группа, обладающая слабой мета-ориентацией. При стабилизации путем превращения в N-ацетиль-ное производное понижается легкость замещения в мета-положение и становится возможным получение орто - и пара-монопроизводных. [33]
 |
Изменение обменной емкости и накопление в продуктах реакции гидроксида три - и тетраметиламмонпя при нагревании АВ-17 X 8 ( ОН . [34] |
Во всехработах по изучению стойкости анионита АВ-17 ( ОН - -) в спиртовых средах отмечается протекание процессов инактивации аммониевых групп с переходом их в состояние, неактивное по отношению к ионному обмену. По данным работы [243], инактивации могут подвергаться до 10 % аммониевых групп анионита АВ-17. Имеющиеся в литературе объяснения причин, инактивации аммониевых групп за счет образования комплексов со спиртами представляются мало убедительными и требуют дальнейшего серьезного изучения. [35]
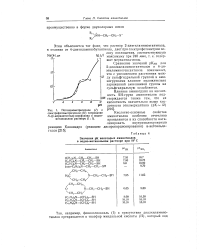 |
Потенциометрическое ( / и спектрофотометрическое ( / / титрование 7У - ( р-меркаптоэтил-морфолина в водно-метанольном растворе. [36] |
Сравнение значений рКзн для 2-диалкиламиноэтантиолов и 6-ди-этиламиногексантиола показывает, что с увеличением расстояния между сульфгидрильной группой и аминогруппами влияние положительно заряженной аммониевой группы на сульфгидрильную ослабляется. [37]
Все эти результаты говорят о том, что пиридиниевая группа оказывает на а-водородные атомы значительно большее активирующее влияние, чем простая аммониевая группа. Это может быть обусловлено стабилизацией карбаниона за счет как электростатического, так и резонансного взаимодействия между карбанионом и пиридиниевым кольцом. [38]
Относительное содержание солей тетраметиламмония и их превышение по сравнению с приращением содержания низкоосновных групп в анионите сильно зависят от ионной формы аммониевых групп и продолжительности нагревания. [39]
Направление реакции определяется наличием орто-пара-ориен-тирующего влияния С1 - атома, так как NH2 - rpynna в среде серной кислоты превращается в аммониевую группу, дезактивирующую орто - и пара-положения по отношению к ней. Поэтому нитрогруппа входит только в положение 3, и в результате нитрования образуется 4-хлор - З - нитроанилин. [40]
Поэтому белки явно обнаруживают амфотерный Характер: карбоксильные группы отщепляют водородные ионы trбелковые ионы приобретают отрицательные заряды, аминогруппы, превращаясь в аммониевые группы, отщепляют гидроксиль-ные ионы и белковые ионы приобретают положительные заряды; в электрическом поле, вследствие этого подобно аминокислотам, яичный белок в водном растворе перемещается к катоду в кислой среде и к аноду - в щелочной среде; естественно, что в изо-электрическом пункте, то есть при рН, соответствующем одинаковой кислотной и щелочной ионизации белка, не происходит перемещения ни к катоду, ни к аноду. [41]
Естественным условием является возможность перегруппировки октет-ной оболочки катиона [ см. ( 2.4, в) ]: это невозможно, например, у аммониевой группы, которая соответственно не проявляет - Af-эффекта. [42]
Обратимся далее к оценкам я-электронных зарядов в орто -, мета - и пара-положениях органического иона, в котором единичный положительный заряд ( например, аммониевой группы NHJ) находится от С-атома кольца на расстоянии 1 42 А по радиальному направлению. Квантрвомеханические расчеты, проведенные Бишопом и Крэйгом [9], а также Чандра и Коулсоном [14], показывают, что наивысший формальный положительный заряд имеет место на атоме углерода в пара-положении. В реакциях с катионами, следовательно, пара-положение должно быть наименее выгодным - опять-таки вывод, не удовлетворяющий опыту. [43]
Обратимся далее к оценкам я-электронных зарядов в орто -, мета - и пара-положениях органического иона, в котором единичный положительный заряд ( например, аммониевой группы NHjJ) находится от С-атома кольца на расстоянии 1 42 А по радиальному направлению. Квантовомеханические расчеты, проведенные Бишопом и Крэйгом [9], а также Чандра и Коулсоном [14], показывают, что наивысший формальный положительный заряд имеет место на атоме углерода в пара-положении. В реакциях с катионами, следовательно, пара-положение должно быть наименее выгодным - опять-таки вывод, не удовлетворяющий опыту. [44]
Фэксторп [436], исходя из бис - ( Р - диметиламиноэтил) - дисульфида, алкилированием бромистым или йодистым этилом получал бис-четвер-тичные соединения, содержащие при атомах азота аммониевой группы метальные и этильные радикалы. [45]
Страницы: 1 2 3 4 5