Ассоциированная группа
Cтраница 2
В том случае, если комплексная молекула содержит ассоциированную группу из молекул пара и удовлетворяется условие ( 324), может произойти непосредственное схватывание ассоциированной группы с поверхностью льда. [16]
В том случае, если комплексная молекула содержит ассоциированную группу, может произойти непосредственное схватывание образовавшейся группы с поверхностью льда. [17]
Надо - будет предположить также, что в ассоциированных группах дипольные моменты ориентируются под углами, близкими к 180, вследствие чего es растворов испытывает отрицательные отклонения от аддитивности. [18]
Теории реальных газов в последнее время используют представления о временных ассоциированных группах. Эти ассоциации особенно сильны вблизи линии насыщения. [19]
Наличие мощных потоков неконденсирующегося газа нарушает образование сублимационного льда из ассоциированных групп молекул пара, не дает возможности ассоциированным группам закрепиться на поверхности или отдельным молекулам образовать кристаллы сублимационного льда. В результате этого коэффициент затвердевания при конденсации пара при вынужденном движении газа оказывается ниже, чем при конденсации пара в неподвижном газе. Вместе с тем интенсивное поступление газа в систему сопровождается заметным повышением температуры движущейся границы сублимационного льда, вызванным теплотой, приносимой в объем конденсатора массой газа. В результате этого ослабляются силы взаимного притяжения в процессе ассоциации молекул пара. Ослабление сил взаимного притяжения при образовании кристаллов облегчает срыв молекул пара с охлаждаемой поверхности потоком воздуха. [20]
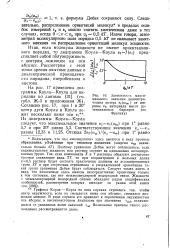 |
Зависимость максимального значения диэлектрических потерь г2 ( ( ат от ширины УО, интервала высот потенциальных барьеров ( по Фрелиху. [21] |
Поэтому уравнения Дебая могут соблюдаться, если индивидуальная жидкость или раствор состоит из одинаковых ассоциированных групп. Так, если компоненты X и У раствора образуют достаточно прочное соединение вида XY, то при концентрации в мольных долях х0 5 раствор будет состоять практически целиком из ассоциированных групп XY и при отсутствии стремления к упорядоченной ориентации таких групп уравнения Дебая будут соблюдаться. Следует также иметь в виду, что излагаемые здесь выводы непосредственно применимы только к тем системам, где нет межмолекулярной водородной связи. [22]
Являются ли эти мицеллы стабильными образованиями с определенной механической прочностью и температурой плавления или диффузными ассоциированными группами молекул углеводородов, покажут будущие исследования. [23]
На основании только что высказанных соображений можно предположить, что в газообразной фазе могут существовать ассоциированные группы молекул НгО, которые оказываются построенными по типу кристаллических тел и, по-видимому, принадлежат к гексагональной системе. [24]
На основании только что высказанных соображений следует признать, что в газообразной фазе могут существовать ассоциированные группы молекул Н2О, которые оказываются построенными по типу кристаллических тел и принадлежат к гексагональной системе. [25]
В отличие от жидкостей в растворах могут изменяться не только размер и средний период жизни ассоциированных групп, но и их состав, ибо они могут слагаться из сольватированных молекул. В этом случае при изменении состава растворителя скорость сольватации и десольватации, определяющаяся скоростью диффузии жидкости и скоростью релаксации сольватных оболочек, будет значительно превышать скорость создания и распада самих групп. Таким образом, при изменении состава среды состав ассоциированных групп будет изменяться практически моментально, а изменения групп, связанные с процессами агрегации или дезагрегации больших молекул, будут протекать значительно медленнее. [26]
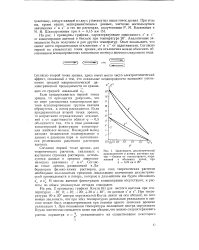 |
Зависимость диэлектрической проницаемости и потерь раствора ацетон - бензол от концентрации, выраженной в объемных долях, при Я 3 21 см и 20. [27] |
Если придерживаться первой точки зрения, то приходится допускать, что по мере уменьшения концентрации ацетона ассоциированные группы сначала образуются, а потом распадаются. Если придерживаться второй точки зрения, то возрастание отрицательных отклонений s от аддитивности вблизи р - 0 5 объясняется тем, что в этом диапазоне концентраций флюктуации концентрации наиболее велики. Последний вывод находит независимое подтверждение в данных о давлении пара и интенсивности релеевского рассеяния растворов ацетона. [28]
Рассматриваемый анионный эффект может быть истолкован аналогичным образом на основе следующих гипотез: а) степень образования ассоциированных групп возрастает в той же последовательности, что и приведенная выше последовательность анионов по анионному эффекту; б) эти группы, которые являются электронейтральными и отличаются слабым взаимодействием с растворителем, очень сильно адсорбируются на границе раздела, где они накапливаются; в) наличие этих групп вызывает ингибирование всех электродных реакций в результате заполнения ими поверхности. Если допустить, что различия в адсорбируемости и в ингибирую-щей способности относительно малы по сравнению с различиями в склонности к ассоциации ( или имеется параллелизм в изменении тех и других величин), можно объяснить почему последовательность возрастания ингибирующего действия совпадает с последовательностью их адсорбционной способности на анионообменной смоле. Возможно, что эффекты, наблюдаемые на границе раздела вода - воздух, обусловлены аналогичными причинами. [29]
Зато другие ионы разрывают существующую структуру с образованием ион-водных комплексов, характеризующихся более однородным ближним порядком, чем ассоциированные группы в чистой воде. В частности, небольшие или многозарядные катионы либо образуют первичные гидратные оболочки, в которых ближний порядок подобен порядку в соответствующих кристаллогидратах, либо делают более жесткой структуру растворителя, удаленного от ионов, в результате чего средняя энергия активации молекул НО увеличивается по сравнению с чистой водой. Такие ионы действуют как положительные гидра-таторы. Большие ионы с низким зарядом также могут разрушать структуру воды с образованием более однородных ион-водных комплексов. Однако в общем случае в растворах, содержащих такие ионы, энергия активации ниже, чем в воде, и, следовательно, большие ионы действуют как отрицательные гидрататоры. [30]
Страницы: 1 2 3 4