Грет-бутильная группа
Cтраница 2
Исследован фотолиз соединений ( 22) - ( 24), Из ( 22) образуется ( 25) и про-дукт расщепления - беязальдегад. Из ( 24) образуются только продукты расщепления, Обсудите, как наличие и конфигурация удаляемой грет-бутильной группы могут влиять на состав продуктов. [16]
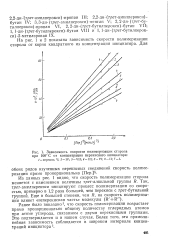 |
Зависимость скорости полимеризации стирола при 100 С от концентрации перекисного инициатора. [17] |
Из данных рис. 1 видно, что скорость полимеризации стирола меняется с изменением величины грег-алкильной группы R. Так, трег-амилперекиси инициируют процесс полимеризации со скоростью, примерно в 1 2 раза большей, чем перекиси с грет-бутильной группой. [18]
 |
Выходы и соотношения изомеров продуктов нитрования некоторых моноалкилбензолов. [19] |
Известно, что индуктивный эффект быстро затухает по цепи а-связей. Однако девять атомов водорода трех метильных групп в грег-бутильной группе, несмотря на большее удаление их от бензольного кольца по сравнению с атомами водорода метиль-ной группы, оказывают более сильное влияние на электронодо-норные свойства грет-бутильной группы, чем три атома водорода в метильной группе. [20]
В табл. 24.4 приведены значения свободных конформационных энергий для заместителей самой различной природы, определенные с помощью ЯМР Ни С при температуре ниже - 100 С. Все галогены имеют низкие и кроме фтора близкие значения ДО0, так как одновременно с ростом объема атома увеличивается длина связи углерод-галоген. Грет-бутильная группа имеет наиболее высокое ДО0, равное 5 4 ккал / моль. При 25 только 1 - 2 молекулы mpem - бутилциклогексана из 10000 т.е. 0 01 % находятся в аксиальной конформаций. [21]
Влияние конформации на реакционную способность особенно подробно научалось для циклогексановых. Различия между аксиальным или экваториальным окружением функциональной группы может привести к значительным различиям в скорости реакции. Наиболее общим путем изучения влияния ориентации на реакционную способность является фиксирование конформации при помощи грет-бутильной группы или другого большого заместителя с целью обеспечить подавляющую предпочтительность экваториальной или аксиальной ориентации реагирующей группы. [22]
Так как присоединение карбоксильной группы всегда протекает строго по правилу Марковникова и карбоксильная группа к конечным атомам углерода не присоединяется, то при нормальном течении реакции количество возможных изомерных кислот может быть определено по формуле Z N - 2, где N - число атомов углерода в исходном олефине. На практике получают большее число кислот, так как в условиях синтеза, особенно при низких давлениях окиси углерода, происходит ди - или олигомеризация исходного олефина, вследствие чего образуется значительное количество высокомолекулярных кислот. С другой стороны, сильная кислота, присутствующая в реакционной смеси, может катализировать расщепление исходных соединений ( особенно легко отщепляются грет-бутильные группы); это приводит к образованию кислот с меньшим числом атомов углерода, чем в исходных веществах. [23]
Хотя все атомы в метанале копланарны, для его высших гомологов наблюдается другая картина. Предпочтительной конформацией этаналя в газовой фазе является заслоненная конформация ( 5); трехступенчатый энергетический барьер для поворота вокруг связи С-1, С-2 имеет величину 4 6 кДж / моль. Для пропана ля и 2-метилпропаналя предпочтительными в каждом случае являются такие конформации, в которых двойная углерод-кислородная связь заслонена метильной группой. Заселенность конформации ( 6) в случае 2-метилпропаналя достигает 90 %; в другом присутствующем в смеси конформере группа С О заслонена атомом водорода. Напротив, в 3, 3-диметилбутанале грет-бутильная группа предпочтительно занимает антиклинальное положение к карбонильной группе, которая заслонена в этом случае атомом водорода. [24]
Следует остановиться на наиболее характерных примерах зависимости химических сдвигов от природы заместителей. Внутри любого из этих трех классов значения сдвигов, связанных с различными функциональными группами, не находятся в соответствии с величинами индуктивного и мезомерного эффектов. Это может быть приписано низкому весу структур ( 13) и ( 17) и структур с растянутыми связями. Больший сдвиг протона 2 - Й в 3-замещенных тиофенах, сравнимый со сдвигом протона 3 - Н в 2-замещенных может быть аналогично объяснен весом соответствующих резонансных структур. Гомологичное замещение мало сказывается на химических сдвигах, за исключением объемной грет-бутильной группы, сильно влияющей на сдвиги протонов кольца. [25]
Джонс [239] приводит значения частот для ряда небольших молекул в газообразном состоянии, а Миядзава и др. [240] провели анализ нормальных колебаний N-метилацет-амида, на основании которого сделали вывод, что полоса амид-1 при 1653 см-1 на 80 % имеет характер карбонильной полосы. Первая группа авторов частично исследовала изотопное замещение N15 и дейтерирование и обнаружила, что vCO не меняется при изотопном замещении атома азота, но смещается на 20 см-1 при дейтерировании. Карбонильные частоты этого ряда соединений лежат вблизи 1650 см-1, но этот вывод основан на измерениях как жидких образцов, так и растворов. Найквист [72, 73], исследовавший сильно разбавленные растворы, указывает узкую область 1687 - 1690 см-1 для всего ряда N-алкилацетамидов при заместителях от метильной до грет-бутильной группы. Карбонильная частота зависит также от природы заместителей в цикле. Томпсон [133] приводит некоторые данные о тех изменениях частоты и интенсивности, которые могут происходить при этом. [26]
Страницы: 1 2