Карбонильная группа - кислота
Cтраница 1
Высокополярная карбонильная группа кислот и их производных может подвергаться нуклеофильной атаке. [1]
Большая стойкость карбонильной группы кислот и чрезвычайно малая способность ее к присоединению по сравнению с более активной карбонильной группой эфиров объясняются следующим образом. В сложных эфирах радикал спирта связан через кислород с карбонильной группой более часто встречающимися в органических соединениях ковалентными связями: это несколько сближает эфиры по свойствам с альдегидами и кетонами. Отрицательный заряд остатка кислоты, как теперь установлено, не связан с определенным атомом кислорода ( стр. [2]
Большая стойкость карбонильной группы кислот и чрезвычайно малая способность ее к присоединению по сравнению с более активной карбонильной группой эфиров объясняются следующим образом. [3]
Большая стойкость карбонильной группы кислот и чрезвычайно малая способность ее к присоединению по сравнению с гораздо более активным поведением карбонильной группы эфиров объясняются следующим образом. В сложных эфирах радикал спирта связан через кислород с карбонильной группой обычными для органических соединений ковалентными связями ( стр. [4]
Большая стойкость карбонильной группы кислот и чрезвычайно малая способность ее к присоединению по сравнению с гораздо более активным поведением карбонильной группы эфиров объясняются следующим образом. В сложных эфирах радикал спирта связан через кислород с карбонильной группой обычными для органических соединений ковалентными связями; что несколько сближает эфиры по свойствам с альдегидами и кетонами. [5]
В ИК-опектрах осадков характерная полоса поглощения карбонильной группы кислот смещается из области 1710 см в область 1680 см, что свидетельствует об образовании связи TL - ОСОО. В спектрах ПМР осадков сигнал протона карбоксильной группы при s / s 10 5 - 12 0 мл, отсутствует, что доказывает протекание реакции замещения атомов водорода при взаимодействии модельных кислот и Ttce, Все исследуемые кислоты и соосадители при разложении осадков регенерируются в неизменном виде. [6]
Давно было замечено, ч: то карбонильная группа кислоты отличается инертностью при реакции восстановления в сравнении с карбонильной группой альдегидов и. [7]
Эти данные согласуются и с механизмом электрофилыгой атаки углерода карбонильной группы кислоты на эфирный кислород дибензоата. Однако в этом случае должны были бы проявиться стерические затруднения, создава-мые о-заместителями в молекуле бмс-фенола, что не соответствует полученным экспериментальным данным. Влияние пространственного эффекта и при ацидолизе незначительно. [8]
Кроме того, сложноэфирная карбонильная группа более реакционноспособна, чем карбонильная группа кислот. [9]
Тогда как с альдегидами и кетопами реакция протекает сравнительно быстро, карбонильная группа кислот с озоном почти не реагирует. [10]
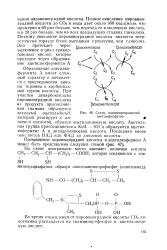 |
Схема взаимопревращений пентозофосфатов. [11] |
Образование ацетилкофермента А имеет сложный характер и начинается с присоединения аниона тиамина к карбонильной группе кислоты. При участии декарбоксилазы пировиноградной кислоты из продукта присоединения тиамина образуется активный ацетальдегид, который реагирует с ли-поевой кислотой, образуя ацетиллипоевую кислоту. Ацетильная группа присоединяется к КоА - SH и образуются ацетил-кофермент А и дигидролипоевая кислота. Последняя вновь окисляется НАД или ФАД до липоевой кислоты. [12]
Было сделано заключение, что олеиновую кислоту можно считать находящейся в хемосорбированном состоянии только в том случае, если полоса при - 5 9 и, обусловленная карбонильной группой кислоты, замещается на полосы при 6 4 и 7 0 ( д, даваемые карбоксильной группой. [13]
Амиды не образуются в этой реакции из-за того, что перенос протона от кислоты ( RC02H) к основанию ( NH3) происходит гораздо быстрее, чем нуклеофильная атака карбонильной группы кислоты аммиаком. После переноса протона отрицательный заряд карбоксилат-иона препятствует атаке любым пуклеофилом. [14]
Экстрагируемые этиловым спиртом стеариновая, олеиновая, абиетиновая, входящая в состав канифоли, синтетические жирные кислоты и др., а также сложные эфиры фталевой, себациносвой кислот идентифицируют методом ИК-спектроскопии, используя различное расположение в ИК-спектре полос поглощения карбонильных групп кислот и эфиров. [15]
Страницы: 1 2