Нулевая группа - периодическая система
Cтраница 1
Нулевая группа периодической системы, состоящая из благородных газов, казалась безупречной. Браш объявил, что плотность этерия составляет всего лишь одну десятитысячную плотности водорода. Вследствие легкости этерия и большой скорости его молекул этот диковинный газ стремится испариться в мировое пространство. [1]
Аргон - элемент нулевой группы периодической системы элементов Д. И. Менделеева, получаемый из жидкого воздуха. [2]
Примечательно, что газы нулевой группы периодической системы ( например аргон) не захватываются металлическими пленками и не являются поэтому промоторами и ядами. Следовательно, захват и включение примесей связаны с химическим актом и с изменением химического состава поверхностного слоя катализатора. Это значит, что захват примеси произойдет тем быстрее и образующееся включение будет тем более устойчивым, чем прочнее будет химическая связь между атомами примеси и решеткой катализатора. [3]
Примечательно, что газы нулевой группы периодической системы ( например аргон) не захватываются металлическими пленками и не являются поэтому промоторами и ядами. Следовательно, захват и включение примесей связаны с химическим актом и с изменением химического состава поверхностного слоя катализатора. Это значит, что захват примеси произойдет тем быстрее и образующееся включение будет тем более устойчивым, чем прочнее будет химическая связь между атомами, примеси и решеткой катализатора. [4]
Многочисленные попытки получения химических соединений элементов нулевой группы периодической системы дали, как известно, в большинстве случаев отрицательные результаты. [5]
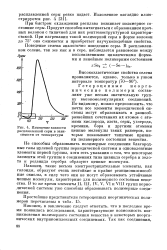 |
Изменение вязкости расплавленной серы в зависимости от температуры. [6] |
Не способны образовывать полимерные соединения благородные газы нулевой группы периодической системы и одновалентные элементы первой группы, хотя есть указания о том, что некоторые элементы этой группы в соединениях типа цианида серебра и золота и роданида серебра образуют цепные молекулы. [7]
Всем этим допущениям ближе всего соответствуют элементы нулевой группы периодической системы, находящиеся в жидком состоянии. [8]
В природных газах установлено присутствие всех представителей нулевой группы периодической системы химических элементов - гелий ( Не), неон ( Ne), аргон ( Аг) криптон ( Кг), ксенон ( Хе) и радон ( Rn) находятся в них в различных количествах. [9]
Атомы в газовой фазе, за исключением атомов элементов нулевой группы периодической системы, неустойчивы и быстро соединяются при тройных столкЕговениях или на стенках сосуда. [10]
Герои этой книги - шесть химических элементов, составляющих нулевую группу периодической системы элементов: гелий, неон, аргон, криптон, ксенон и радон. В ней рассказывается о строении атомов, изотопах и необычайных свойствах этих газов; о том, как основное их свойство - химическая недеятельность - нашло ценные применения в ряде отраслей техники; как были открыты инертные газы, как получают их в промышленности, какие научные открытия и достижения в технике связаны с ними. Из этой книги читатель узнает о распространении инертных газов на Земле и в космосе и как они помогают раскрывать тайны мироздания и историю Земли. Узнает также о роли этих газов в познании строения атома и ядерных превращений. [11]
Основная идея настоящей работы заключается в том, что изучение молекулярных соединений элементов нулевой группы периодической системы - инертных газов - должно сыграть ведущую роль для выяснения законов образования всей группы молекулярных соединений. Инертные газы ( особенно тяжелые) должны давать молекулярные соединения, поскольку они обладают заметными ван-дер-ваальсовыми силами. Среди других веществ они являются простейшими, так как молекулы их одноатомны и наиболее симметричны как в геометрическом, так и в электростатистическом отношении. Они ведут себя, как сферы, и не обладают постоянным дипольным моментом. Следовательно, их молекулярные соединения должны быть идеальным прообразом молекулярных соединений других веществ. Сравнивая поведение инертных газов и других веществ при образовании молекулярных соединений с каким-нибудь третьим веществом, можно решить вопрос о том, какую роль играет здесь число атомов в молекуле, ее геометрическая форма и наличие дипольного момента. Такой подход к изучению молекулярных соединений может показаться с первого взгляда парадоксальным, так как, несмотря на долголетние поиски химических соединений инертных газов, удалось открыть для них только три гидрата. Принято считать, что они в химическом отношении практически совершенно недеятельны. Однако, как показано ниже, высказанные идеи вполне оправдываются на опыте. Соединения инертных газов искали до сих пор не там, где нужно. [12]
 |
Сопоставление энергетических. [13] |
Из сказанного видно, что нейтральная молекула СеН6 сходна по поведению с атомами инертных газов нулевой группы Периодической системы Д. И. Менделеева: этим атомам отвечают особо устойчивые замкнутые в себе симметричные оболочки из восьми электронов. [14]
Согласно Льюису, группы из двух или восьми электронов чрезвычайно устойчивы, чем и объясняется химическая инертность элементов нулевой группы периодической системы. По этой теории, атом гелия имеет два электрона, атом неона также два электрона, расположенных внутри куба, образованного восемью электронами. В аргоне еще восемь электронов расположены в вершинах куба, внешнего по отношению к кубу неона. Атомы различных элементов стремятся к захвату или к отдаче электронов, так чтобы приобрести при этом сходство с гелием или другим элементом нулевой группы. [15]
Страницы: 1 2 3