Гунда
Cтраница 1
Гунда, необходимо предположить, что иаииизшим по энергии состоянием, возникающим из каждой конфигурации, будет спиновый триплет. [1]
Гунда правило - правило, утверждающее, что наиболее устойчивой конфигурацией среди нескольких возможных с одинаковой орбитальной энергией является та, которая содержит наибольшее число не-спаренных электронов. [2]
 |
Схема образования из. [3] |
Гунда): Они-то и являются виновниками парамагнетизма молекулы кислорода. Таким образом, в ММО парамагнетизм Оа обоснован строго научно и нет необходимости в постулировании трехэлектронной связи. [4]
Гунда используются квантовые числа N ( вместо /) и S. Квантовое число ( /) используется для классификации уровней по типам симметрии молекулярной группы вращений. [5]
Гунда; - в атомных спектрах основной терм ассоциируется с максимальной мультиплетностью, возможной для данной электронной конфигурации; вообще, наинизшим энергетическим состоянием атома или иона считается такое, при котором максимальное число электронов, допускаемое принципом Паули, имеет неспаренные спины; одно из правил, используемых в сочетании с принципом Паули при расшифровка спектров многоэлектроиних атомов и ионов. [6]
Гунда: при последовательном заполнении орбиталей одного и того же энергетического уровня размещение на любой из них двух электронов возможно лишь после того, как на каждой орбитали будет хотя бы по одному электрону. [7]
Гунда, они должны быть неспарены. [8]
Гунда, необходимо предположить, что наинизшим по энергии состоянием, возникающим из каждой конфигурации, будет спиновый триплет. [9]
Гунда: на данном подуровне электроны стремятся занять максимальное число свободных атомных орбиталей. [10]
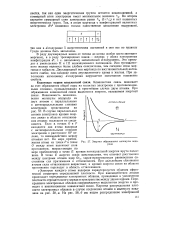 |
Энергия образования молекулы водорода. [11] |
Гунда должны быть заполнены. [12]
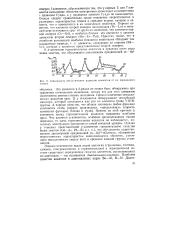 |
Зависимость металлических радиусов элементов от их порядкового номера. [13] |
Гунда, а у последних правило Гунда не выполняется. Отсюда следует сравнительно малое изменение энергетических и размерных характеристик атомов в середине вторых пятерок и семерок, что и проявляется в их химических свойствах. Bk - Lr), которые и являются представителями второй семерки. [14]
Гунда) электрона на трехкратно вырожденном яр-уровне. Однако между элементами этой группы существуют и различия в электронном строении. Так, у фосфора в отличие от азота впервые появляется вакантный внешний Зй-уровень, что обусловливает возможность промотирования одного Ss-электрона с образованием пятиковалентного состояния, которое, как известно, отсутствует у азота. У мышьяка, сурьмы и висмута к вакантному nd - уровню добавляется еще в отличие от фосфора полностью завершенный внутренний ( п - 1) й-уровень, а у висмута, следующего за лентаноидами, кроме того, и 4 / 14-уровень. [15]
Страницы: 1 2 3 4