Давление - пар - аммиак
Cтраница 1
Давление пара аммиака над растворами боргидрида в нем при температурах от - 49 8 до 95 С показано на рис. X. На изотермах отмечаются характерные площадки, соответствующие образованию отдельных аммиакатов. [1]
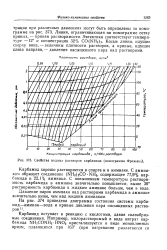 |
Свойства водных растворов карбамида ( номограмма Фрежака. [2] |
Давление паров аммиака над растворами карбамида в аммиаке значительно ниже, чем над жидким аммиаком. [3]
Давление паров аммиака над растворами мочевины в аммиаке значительно ниже, чем над жидким аммиаком. [4]
Давление пара аммиака над такими растворами значительно ниже, чем над концентрированными растворами, и благодаря этому потери аммиака значительно уменьшаются. [5]
Зная, что давление пара аммиака при обычной температуре довольно велико, вы можете предположить, что при внесении аммиака в почву часть его испаряется и безвозвратно теряется. Однако оказывается, что при внесении жидкого аммиака в почву на глубину 10 - 15 см он быстро поглощается частицами почвы и не улетучивается. По эффективности жидкий аммиак ( в расчете на единицу азота) не уступает твердым азотным удобрениям. [6]
 |
Значения параметра CTI / PI, характеризующего эффективность заполнения фитиля, от температуры пара. [7] |
При указанной температуре давление паров аммиака и ацетона составляет 11 5 и 1 7 МПа соответственно. [8]
Определены условия, при которых давление паров аммиака в процессе дис-социац ш ортофосфатов может быть уравновешено давлением газообразного аммиака. Большая часть воды моноаммонийфосфата удаляется в интервале температур 275 - 325 С, после чего дегидратация замедляется. Состав получающихся продуктов близок к составу высокомолекулярных полифосфатов. Исследовано также влияние на состав дегидратированных фосфатов таких факторов, как давление водяных паров над реакционной массой, продолжительность аммонизации, скорость охлаждения плава и присутствие модифицирующих примесей. [9]
Одни из них [1] предлагают метод расчета давления паров аммиака и двуокиси углерода, сходный с описанным выше методом для аммиачных растворов, содержащих сероводород. [11]
На этом же рисунке нанесена и кривая, характеризующая давление паров аммиака. Так, давление HCI при рН около 2 2 составляет 16 53 гПа, а при рН близком к 3 2 снижается до 0 4 гПа, при рН 4 0 пары НС1 в газовой фазе практически отсутствуют. [12]
Из таблицы видно, что наиболее растворим в воде диаммонийфосфат, давление паров аммиака выше над триаммонийфосфатом. В процессе сушки моноаммоний-фосфата при 100 - 105 С не наблюдается потерь аммиака. [13]
В отключенном испарителе за счет притока тепла от окружающего воздуха температура и давление паров аммиака постепенно повышаются. В момент подключения к работающей системе в нем происходит резкое снижение давления и бурное кипение оставшегося жидкого аммиака, в результате чего жидкость может попасть во всасывающий трубопровод и в цилиндр компрессора. [14]
В случае амминов меди удовлетворительные и воспроизводимые результаты были получены при измерении давления паров аммиака и светопоглощения, а также при использовании медного электрода. Однако применение этих методов было связано с довольно длительной и трудоемкой работой. Поэтому использование стеклянного электрода в качестве универсального прибора для быстрого и удовлетворительного исследования процесса образования амминов в растворе оказалось исключительно прогрессивным. Рассмотрим этот вопрос более подробно. [15]
Страницы: 1 2 3 4