Давление - пар - растворенное вещество
Cтраница 1
Давления паров растворенных веществ над разбавленными растворами очень малы и трудно измеримы. Поэтому целесообразно изучать реакции, в которых данный компонент образует газообразный продукт. [1]
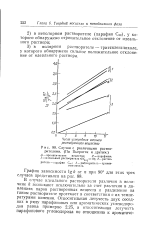
Рассмотрим теперь давление пара растворенного вещества в разбавленном растворе, например сероуглерода в метилале, в ту область малых концентраций сероуглерода, в которой растворитель ( метилаль) еще полностью следует закону Рауля. [2]
Таким образом, давление пара растворенного вещества в стандартном состоянии должно быть численно равно константе Генри. [3]
Закон пропорционального изменения давления пара растворенного вещества с изменением его концентрации в растворе впервые был найден английским химиком Генри при изучении растворимости газов и назван законом Генри. В применении к растворимости газов в жидкостях он формулируется так: при постоянной температуре растворимость данного газа в жидкости прямо пропорциональна его давлению над жидкостью. [4]
Причем предполагается, что давление пара растворенного вещества над раствором настолько низкое, что этот пар можно считать идеальным. Понятно, что согласно закону Рауля концентрации должны быть выражены в молярных долях. [5]
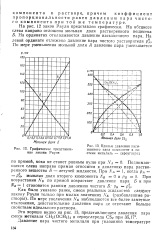
Рассмотрим определение коэффициентов активности по давлению пара растворенного вещества: например, коэффициентов активности хлористого водорода в водном растворе. [6]
 |
Графическое представление закона Рауля.| Кривые давления насыщенного пара компонент в системе метилаль - сероуглерод. [7] |
Поднимающаяся слева направо прямая относится к давлению пара растворенного вещества Б - летучей жидкости. [8]
Следовательно, в идеальном предельно разбавленном растворе давление пара растворенных веществ пропорционально их мольной доле в растворе. Этот закон называется законом Генри, а &, - постоянными Генри. [9]
Следует помнить, что насыщенный раствор имеет такое же давление пара растворенного вещества, как и кристаллическое вещество, находящееся в равновесии с насыщенным раствором. [10]
В реальных растворах, которые не являются уже предельно разбавленными, давление пара растворенного вещества в большей яли меньшей степени уклоняется от закона Генри. [11]
К прямым методам относится определение коэффициентов активности: 1) по давлению пара растворенного вещества; 2) по распределению вещества между двумя несмешивающимися жидкими фазами; 3) по распределению вещества между жидкой и поверхностными фазами ( адсорбция); 4) по электродвижущей силе цепей без переноса и с переносом. [12]
B еих пробах, если молекулярная масса растворителя составляет 100, а давление пара растворенного вещества P t при температуре колонки равно 2 0 мм. [13]
В случае идеального растворителя различия в величине k возникают исключительно за счет различия в давлениях паров растворенных веществ и разделение на таком растворителе протекает в соответствии с их температурами кипения. [15]
Страницы: 1 2 3