Давление - пар - чистое вещество
Cтраница 2
 |
Относительные отклонения вычисленных давлений паров от экспериментальных при корреляции данных с помощью уравнения NRTL в системе бензол ( / - циклогек. [16] |
Последний пример показывает, как важно при оценке параметров уравнений для коэффициентов активности использовать надежные данные о давлении паров чистых веществ. [17]
Эта ситуация принципиально отличается от наблюдаемой в ГХ, где определяющими факторами являются взаимодействие с неподвижной фазой и давление паров чистого вещества ( образца) ( см. разд. [18]
Выражения ( 4) были получены в результате обработки при помощи уравнения ( 1) экспериментальных данных о давлении паров чистых веществ в условиях термодинамического равновесия с жидкостью. [19]
Вследствие отрицательного отклонения от закона Рауля удерживаемые объемы этих углеводородов обычно выше, чем можно было бы предсказать на основании давлений паров чистых веществ. В случае полярных растворенных веществ в значительной степени может иметь место обратный эффект. [20]
Если XAI, то есть речь идет о чистом веществе А, то рА К - р А, т есть давлению пара чистого вещества при данной температуре. [21]
Числовые значения коэффициентов в выражении для m были получены в результате обработки при помощи уравнения ( 106) экспериментальных данных о давлении паров чистых веществ в условиях термодинамического равновесия с жидкостью. [22]
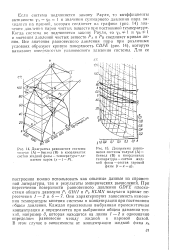
Если система подчиняется закону Рауля, то коэффициенты активности - YB 1 и значения суммарного давления пара находятся на прямой, которая соединяет па графике ( рис. 14) значения давления паров чистых веществ при постоянной температуре. РА и РВ соединяет кривая линия. Все значения равновесного давления пара при различных условиях образуют кривую поверхность CDFE ( рис. 14), которую называют поверхностью равновесного давления системы. [24]
Так как для чистого вещества парциальный мольный объем есть просто мольный объем и он всегда положителен, а объем пара 12п больше объема жидкости VZB, то производная в уравнении ( 56) является отрицательной. Этот результат хорошо известен [6] и означает снижение давления пара чистого вещества, находящегося в смачиваемой им пористой среде. [25]
Опыт и теория показывают, что в области предельно малых концентраций растворенного вещества все же существует закон пропорциональной зависимости между давлением пара растворенного вещества и его мольной долей в растворе. Однако коэффициент пропорциональности в общем случае не равен давлению пара чистого вещества Б, а может быть больше или меньше его в зависимости от характера уклонения системы от свойств идеального раствора. [26]
Если выполняется закон Рауля ( идеальная смесь), то pixlpi, где pi - давление пара чистой жидкости. Таким образом, для идеальной смеси летучесть компонента просто равна давлению пара чистого вещества. [27]
РА - парциальный поток компонента А в паровой фазе; Р - общий поток через систему; Рд - давление насыщенных паров чистого вещества А при температуре системы; уд - коэффициент активности, которым уравнение (13.14) отличается от аналогичного уравнения, справедливого для идеального раствора. Уравнение (13.14), разумеется, выполняется только для низких давлений ( содержание в стандартном жидком состоянии задается давлением паров чистого вещества при данной температуре системы) до 1 атм, что достаточно для наших целей. [28]
Для идеальных смесей ( и чистых веществ) летучесть при постоянной температуре не зависит от состава раствора и равна давлению пара чистого вещества, а относительная летучесть - отношению давлений чистых компонентов. [29]
Характерным признаком идеальных растворов является строгое подчинение их закону Рауля, согласно которому давление пара вещества А над раствором равно давлению пара чистого вещества РА, умноженному на его мольную долю в растворе. Закон Рауля применяют для вычисления свойств бесконечно разбавленных растворов. [30]
Страницы: 1 2 3