Относительное давление
Cтраница 2
Измерив относительное давление пара растворителя над раствором или студнем с известной концентрацией полимера с молекулярной массой М, нетрудно вычислить величину / С, а затем и молекулярную массу термодинамического сегмента Мт М / К. [16]
Значение относительного давления важно знать при промывке фонтанных скважин, при производстве других ремонтных работ, а также при восстановлении скважин методом зарезки и бурения второго ствола для того, чтобы правильно выбирать плотность бурового раствора. [17]
 |
График изменения относи - Н3 Относительных ДЗВЛеНИЙ ПО.| Зависимость коэффициента Л6НИЯ МОЖНО ИСПОЛЬЗОВать. [18] |
Величина относительного давления в форме в этот период превосходит относительное давление в период заполнения формы. [19]
Зависимость относительного давления паров растворителя над раствором полимера от мольной доли растворителя подчиняется закону Рауля. [20]
 |
Зависимость давления пара растворителя над раствором полимера от мольной х ( а и объемной ф ( б доли компонентов. [21] |
Зависимость относительного давления пара растворителя от состава раствора полимера имеет различный вид, смотря по тому, в мольных или объемных долях выражен состав. Если выражать состав в мольных долях, то кривая проходит почти по осям координат ( рис. 11.2 а), т.е. раствор полимера характеризуется резко отрицательными отклонениями от идеальности. Однако в данном случае это не означает, что компоненты очень хорошо смешиваются. Такой вид кривой является результатом огромной разницы в размерах молекул компонентов, вследствие чего мольная доля растворителя в растворах практически любой концентрации близка к единице. [22]
Зависимость относительного давления пара растворителя над раствором полимера от мольной доли растворителя подчиняется закону Рауля. [23]
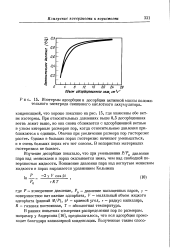 |
Изотермы адсорбции и десорбции активной массы положительного электрода свинцового кислотного аккумулятора. [24] |
При относительных давлениях выше 0 5 десорбционная ветвь лежит выше, но она снова сближается с адсорбционной ветвью в узком интервале размеров пор, когда относительные давления приближаются к единице. Обычно при увеличении размера пор гистерезис растет. Однако в больших порах гистерезис начинает уменьшаться, и в очень больших порах его нет совсем. В непористых материалах гистерезиса не бывает. [25]
При относительном давлении 0 2 на поверхности твердого тела адсорбируется примерно 1 - 2 монослоя газа. [26]
При относительных давлениях, больших 0 35 и вплоть до 0 50, экспериментальные данные, представленные по уравнению ( 38), с ростом давления все более и более отклоняются от прямой линии. Поэтому становится необходимым пользоваться уравнением ( 41), содержащим три константы. Это иллюстрируется на рис. 71, на котором изображена изотерма адсорбции азота при 77 3 К на железном катализаторе, промотированном окисью алюминия. Следует отметить, что для относительных давлений, меньших 0 35, все четыре изотермы совпадают, и расхождения начинаются только при более высоких относительных давлениях. [27]
При относительном давлении 0 2 на поверхности твердого тела адсорбируется примерно 1 - 2 монослоя газа. Предположим, что в данном случае I м поверхности покрыт монослоем газа. [28]
При относительных давлениях, превышающих 0 2, пористые адсорбенты десорбируют пара больше, чем адсорбируют. Предложено несколько вариантов объяснения этих типов гистерезиса. Жигмонди [20] предположил, что в процессе адсорбции пары не полностью смачивают стенки капилляров адсорбента, так как примеси типа воздуха могут постоянно адсорбироваться на стенках пор. Повышение давления приводит к вытеснению любых примесей до тех пор, пока при давлении насыщенного пара адсорбата не будет иметь место полное смачивание стенок. При десорбции краевой угол в уравнении Кельвина равен нулю. [29]
При относительных давлениях, больших 0 35 и вплоть до 0 50, экспериментальные данные, представленные по уравнению ( 38), с ростом давления все более и более отклоняются от прямой линии. Поэтому становится необходимым пользоваться уравнением ( 41), содержащим три константы. Сначала определяются значения vm и с графически по уравнению ( 38) для р / р0 0.35, а затем, пользуясь найденными значениями, с помощью уравнения ( 41) определяют методом последовательных приближений значение п, дающее наилучшее согласие с экспериментальными данными. Это иллюстрируется на рис. 71, на котором изображена изотерма адсорбции азота при 77 3 К на железном катализаторе, промотированном окисью алюминия. Следует отметить, что для относительных давлений, меньших 0 35, все четыре изотермы совпадают, и расхождения начинаются только при более высоких относительных давлениях. [30]
Страницы: 1 2 3 4 5