Осмотическое давление
Cтраница 2
Осмотическое давление численно характеризует осмотические свойства раствора ( см. гл. Под осмотическим давлением понимается дополнительное давление ( точнее разность давлений за мембраной), которое необходимо приложить к раствору, чтобы осмос прекратился. Это достигается при сходстве компонентов. [16]
Осмотическое давление возникает на контакте двух растворов с разной минерализацией, разделенных полупроницаемой перегородкой; оно тем выше, чем больше разность концентраций. В скважине роль полупроницаемой перегородки выполняет фильтрационная корка, образующаяся на проницаемых стенках. [17]
 |
Разность уровней, обусловленная осмотическим давлением. [18] |
Осмотическое давление оказывается довольно значительным даже при весьма малых концентрациях растворенных веществ. [19]
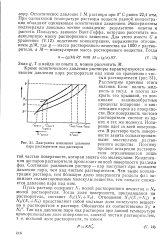 |
Диаграмма изменения давления пара растворителя над раствором. [20] |
Осмотическое давление 1 М раствора при 0 С равно 22 4 атм. При одинаковой температуре растворы веществ равной концентрации обладают одинаковым осмотическим давлением. [21]
Осмотическое давление, закон Вант-Гоффа, температуры кипения и замерзания растворов и закон Рауля связаны с движением и концентрацией частиц растворенного вещества. Очевидно, все закономерности, определяющие физические свойства растворов, имеют общую основу. Такой общей основой является соотношение числа частиц растворенного вещества и растворителя в растворе. [22]
Осмотическое давление подчиняется газовым законам, поэтому для его вычисления можно воспользоваться уравнением Клапейрона - Менделеева PV RT, несколько видоизменив его. В этом уравнении V - объем раствора, который содержит 1 моль растворенного вещества. [23]
Осмотическое давление подчиняется газовым законам, поэтому для его вычисления можно воспользоваться уравнением Клапейрона - Менделеева PV - RT, несколько видоизменив его. В этом уравнении V - объем раствора, который содержит 1 моль растворенного вещества. [24]
Осмотическое давление подчиняется газовым законам, поэтому для его вычисления можно воспользоваться уравнением Клапейрона - Менделеева PV RT, не сколько видоизменив его. В этом уравнении У - объем раствора, который содержит 1 моль растворенного вещества. [25]
Осмотическое давление не зависит от природы полупроницаемой перегородки. Если бы это было не так, можно было бы осуществить перпетуум мобиле, поместив раствор между двумя разными мембранами, после чего в чистых растворителях, находящихся по другую сторону от каждой мембраны, можно было бы констатировать различное давление. Однако, согласно второму закону термодинамики, это невозможно. [26]
Осмотическое давление описывается газовым законом, поэтому для его вычисления можно воспользоваться уравнением Клапейрона - Менделеева PV - RT, несколько видоизменив его. В этом уравнении V - объем раствора, который содержит 1 моль растворенного вещества. [27]
 |
Зависимость давления пара над раствором полистирола от весовой доли компонентов. [28] |
Осмотическое давление в растворах полимеров является функцией концентрации раствора, но даже в очень разбавленных растворах уравнение Вант-Гоффа не соблюдается. [29]
Осмотическое давление измеряется в приборах, называемых осмометрами. [30]
Страницы: 1 2 3 4