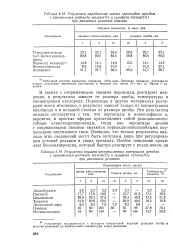
Алкилгидропероксид
Cтраница 2
Решающим фактором в увеличении селективности окисления насыщенных углеводородов ( повышении выхода спиртов с неизменным углеродным скелетом) в присутствии борной кислоты и алкилборатов является действие названных соединений бора на распад гидропероксида. Борная кислота и ее эфиры увеличивают скорость разложения алкилгидропероксидов и способствуют образованию спиртов. [16]
Основный растворитель может связывать Я-кислоту - катализатор, понижая эффективность ее действия, или блокировать электро-фильный центр кислоты Льюиса, конкурируя с нуклеофильным реагентом. Примером может служить ингибирующее влияние спиртов и воды на эпоксидирование олефинов алкилгидропероксидами в присутствии соединений металлов с переменной валентностью. На первой стадии этого процесса алкилгидропероксид, как нуклеофил, образует с катализатором донорно-акцепторный комплекс. [17]
Большинство гидропероксидов - жидкости, некоторые из них - кристаллические твердые вещества; как правило, они имеют несколько более низкие точки плавления и более высокие точки кипения, чем соответствующие спирты. Растворимость гидропероксидов в воде и органических растворителях напоминает растворимость соответствующих спиртов / Кроме двух первых членов гомологического ряда алкилгидропероксиды в чистом состоянии достаточно устойчивы и могут перегоняться или плавиться ниже 70 С, однако при более высоких температурах с ними следует обращаться с большой осторожностью, поскольку они способны разлагаться со взрывом. Примеси, такие как ионы металлов, пыль и инертные частицы, вызывают очень значительную и часто трудно объяснимую потерю устойчивости. Гидропероксиды являются несколько более сильными кислотами, чем соответствующие спирты, поэтому их иногда отделяют в виде солей щелочных металлов от нейтральных примесей, например алканов, алкенов, спиртов, простых эфиров и карбонильных соединений. [18]
Основный растворитель может связывать Я-кислоту - катализатор, понижая эффективность ее действия, или блокировать электро-фильный центр кислоты Льюиса, конкурируя с нуклеофильным реагентом. Примером может служить ингибирующее влияние спиртов и воды на эпоксидирование олефинов алкилгидропероксидами в присутствии соединений металлов с переменной валентностью. На первой стадии этого процесса алкилгидропероксид, как нуклеофил, образует с катализатором донорно-акцепторный комплекс. [19]
Фишеру, эта абсорбция приписывается образованию перекиси хлорофилла. Фишер изображает ее в виде алкилгидропероксида Е - О-ОН с пероксидной группой в положении 10 ( см. формулу на стр. Некоторые затруднения в этой гипотезе, в частности тот факт, что абсорбция кислорода может наблюдаться лишь в спирте, будут рассмотрены в главе XVI. Пока еще окончательно не доказано, что поглощение кислорода при алломеризации обратимо. [20]
Большинство гидропероксидов - жидкости, некоторые из них - кристаллические твердые вещества; как правило, они имеют несколько более низкие точки плавления и более высокие точки кипения, чем соответствующие спирты. Растворимость гидропероксидов в воде и органических растворителях напоминает растворимость соответствующих спиртов. Кроме двух первых членов гомологического ряда алкилгидропероксиды в чистом состоянии достаточно устойчивы и могут перегоняться или плавиться ниже 70 С, однако при более высоких температурах с ними следует обращаться с большой осторожностью, поскольку они способны разлагаться со взрывом. Примеси, такие как ионы металлов, пыль и инертные частицы, вызывают очень значительную и часто трудно объяснимую потерю устойчивости. Гидропероксиды являются несколько более сильными кислотами, чем соответствующие спирты, поэтому их иногда отделяют в виде солей щелочных металлов от нейтральных примесей, например алканов, алкенов, спиртов, простых эфиров и карбонильных соединений. [21]
В диенах с сопряженными связями пероксиды реагируют медленно, и результаты зависят от размера пробы, температуры и концентрации кислорода. Пероксиды в других материалах реагируют почти мгновенно, и результат зависит только от концентрации кислорода и в меньшей степени от размера пробы. Эти результаты анализа согласуются с тем, что пероксиды в моноолефинах и, вероятно, в простых эфирах представляют собой реакционноспо-собные алкилгидропероксиды, тогда как пероксиды диенов с сопряженными связями являются нереакционноспособными пер-оксидами мостикового типа. Очевидно, что точные результаты анализа этих соединений могут быть получены лишь при регулировании условий реакции в узких пределах. [23]
Органические гидропероксиды являются обычно очень реакци-онноспособными соединениями; кислород-кислородная связь легко разрывается гомолитически, давая один или несколько продуктов в зависимости от условий окисления и строения алкана. Газофазное окисление вследствие значительно меньшей селективности имеет меньшее значение в химической промышленности, чем жидкофаз-ное окисление. Важнейшим промышленным применением жидко-фазного процесса является производство уксусной кислоты из бутана или низкокипящих нефтяных фракций. В ходе этого процесса образующиеся при разложении алкилгидропероксидов алкоксира-дикалы диспропорционируют с разрывом С-С - связи, давая этиль-ные радикалы и ацетальдегид, который далее окисляется в уксусную кислоту. [24]
Страницы: 1 2