N-ацилирование
Cтраница 2
Отклонимся ненадолго от предмета нашего изложения, чтобы рассмотреть некоторые реакции N-ацилирования, в которых реагент генерируется в ходе процесса МФК - Если к смеси водного раствора солей щелочных металлов органических кислот, амина и быс - ( о-нитрофенил) фенилфосфоната в СР СЬ добавить при перемешивании небольшое количество Bu4NX, то экстрагирующиеся карбоксилат-ионы превращаются в смешанный ангидрид, являющийся промежуточным продуктом. Аналогично можно получить р-лактамы из N-бензил-р - аминокислот, проводя дегидратацию через промежуточное образование смешанных ангидридов с метансульфонилхлоридами в системе водный КНСОз / хлороформ / 15 мол. [16]
Защита карбоксильной группы может быть осуществлена этерифйкацией, а аминогруппы - N-ацилированием и N-фтораци-лированием. Одновременно амино - и карбоксигруппы могут быть защищены получением алкилсилилпроизводных аминокислот. [17]
Хотя в предыдущих двух разделах этой главы уделялось внимание гидролитическим процессам, Сыли рассмотрены я два механизма, приводящие к О - и N-ацилированию. При обсуждении катализируемого кислотой гидролиза сложных эфиров было отмечено, что данная реакция обратима. [18]
N-ацилирование / / Материалы VI Международной научно-технической конференции при VI Международной специализированной выставке Строительство, архитектура, коммунальное хозяйство-2002. [19]
Получение феноксиметилхлоридов описано на стр. Солеобразовани: ( среда - ьшнеральпая нислота), N-ацилирование и N-алкилирование снижают ело мбность ароматических аминов вступать в реакцию с галогенами. Взаимодействие с галогенами подвергают водные растворьь гндрогалогенидов аминов или применяю в качестве растворителя ледяную уксусную кислоту t и иоторой для связывании обра дующегося галогеноводорода добавляют ацетат натрия. Так же нак при бромнровэ дни фенолов, особенно большой интерес представляет получение мопо - и дибромдро взводных аминов. [20]
Ацилирование спиртов приводит к сложным эфирам и называется О-ацилиро-ванием. Ацилирование аммиака, первичных и вторичных аминов приводит соответственно к амидам, N-алкиламидам и N, N-диалкиламидам и называется N-ацилированием. [21]
Первичные и вторичные амины гладко реагируют с галогенангидридами и ангидридами кислот. В результате ацилирования аминов образуются амиды кислот. Эти реакции известны как N-ацилирование аминов. [22]
 |
Продукты ацилирования первичных амидов RCONH2 [ схему. [23] |
При использовании этих агентов протекание реакции настолько облегчается, что ее можно проводить при очень низких температурах ( - 60 С) с целью избежать образования нитрила. Однако часто проходит более глубокое ацилирование, что приводит к триацил-аминам. Это означает, что O - - N-перегруппировка интермедиата ( 45) [ направление ( а) на схеме ( 86) ] при низкой температуре Протекает очень медленно, в то время как N-ацилирование ( 45) направление ( б) на схеме ( 86) все-таки протекает, что дает три-ациламины. Напротив, при комнатной температуре О - - перегруппировка ( 45) протекает легко, и если используется несильный ацилирующий агент [102], дальнейшая реакция с образованием триациламина не происходит. [24]
Сфингомиелины, биосинтез - ферментативное образование сфингомиелинов, которое обеспечивается двумя метаболическими путями. Его предшественниками служат церамид и ЦДФ-холин. По второму пути Сфингомиелины синтезируются за счет N-ацилирования сфинганилфосфорилхолина. Взаимоотношение между отдельными путями биосинтеза сфингомиелинов приведено на схеме. [25]
Из рассмотрения этих схем следует, что О-ацилирование должно приводить к освобождению 1 моля я-нитрофенолят-иона и протонов, а М - ацилирование - к освобождению 1 моля п-нитрофе-нолят-иона и протонов и некоторой части от моля протонов в зависимости от того, насколько полно при рН реакции протони-руется фермент. В действительности, концентрация п-нитрофено-лят-иона возрастает, указывая на общее уменьшение количества протонов из буфера. При рН 6 6 белок захватывает около 0 5 моля протонов на 1 моль фермента. Авторы считают, что это противоречит механизму, включающему N-ацилирование, но согласуются с механизмом, включающим О-ацилирование, сопровождающееся изменением величины р / С некоторой основной группы фермента. [26]
Помимо описанной выше рацемизации, для превращения L-трео-ами - нов ( 112) в DL-грео-соединения ( 112 115) был также предложен многостадийный способ, основанный на последовательном уничтожении в молекуле обоих асимметрических центров и создании их заново. Последние в результате присоединения НС1 или МеОН и восстановления NaBH4 образуют DL-эрыгро-ацил. ОМе) 127 - 851 - 857 - 291) - 1292, превращение которых в Д1 - трео-1 - арил-2 - аминопропан-1 3-диолы было рассмотрено в предыдущем разделе. Кроме того, D - p - ацилоксипро-пиофеноны ( 120) можно путем кислотного гидролиза с последующим N-ацилированием превратить в D - p - оксипропиофеноны ( 114) 12 /, мв, 84 /, 858 859 и затем рацемизовать их, как описано выше; однако этот обходный путь вряд ли имеет практическое значение. [27]
Эледоизин понижает артериальное давление у человека, но его передозировка ведет к учащению дыхания. Эледоизин можно фармакологически отличить от кининов плазмы благодаря качественным и количественным особенностям его действия как in vivo, так и in vitro. Гипотензивный эффект держится дольше, чем в случае брадикинина. При подкожном введении повышается секреторная активность слюнных желез и желез слизистой желудочно-кишечного тракта. Из структурно-функциональных исследований следует, что нона - и декапептид в два раза более активны, чем на-тивный гормон, а С-концевой гептапептид обладает полной активностью гормона. Активные аналоги могут быть получены N-ацилированием некоторых пента - и гексапептидных фрагментов. [28]
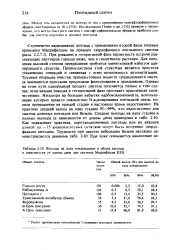 |
Выходы на одну конденсацию и общие выходы в зависимости от длины цепи при синтезах Меррифилда. [29] |
Ступенчатое наращивание пептида с применением второй фазы впервые проведено Меррифилдом на примере твердофазного пептидного синтеза ( разд. Для получения высокой степени превращения требуется значительный избыток аци-лирующего средства. Преимуществом этой стратегии является простота технических операций и связанная с этим возможность автоматизации. Трудные операции очистки промежуточных веществ традиционного синтеза заменяются простыми процессами фильтрования и промывания. Однако на этом пути однородный продукт синтеза получается только в том случае, если каждая реакция в гетерогенной фазе протекает практически количественно. Несмотря на большие избытки карбоксикомпонента, использование которых чревато опасностью N-ацилирования пептидной связи, полное превращение на каждой стадии в настоящее время недостижимо. На практике средний выход на одну стадию 95 - 99 %, что недостаточно для синтеза длинных пептидов или белков. Как показывает практика, короткоцепочечные пептиды или их аналоги длиной до - 15 аминокислотных остатков могут быть получены твердофазным методом. [30]
Страницы: 1 2