Алкилолов
Cтраница 2
Продукты частичного алкилирования RnSnX4 n из ди-и тригалогенидов алкилолова образуются с хорошим выходом. [16]
Конструирование и использование препаративных газовых хроматографов для получения чистых соединений алкилолова, бензола и циклогекоава для радиационнохимических целей. [17]
Алкильные производные олова не разрушаются водой при температуре до 100 С, Галогениды алкилолова и гидроокиси растворимы в воде; галоге-ниды дают проводящие ток растворы, в которых они частично и обратимо гид-ролизованы. [18]
 |
Токсикологическая оценка некоторых ООС. [19] |
Первые обычно недостаточно универсальны, часто не характеризуются высокой эффективностью, а поэтому сочетаются с S-содержащими ООС, которые ( в частности, тиогликоляты и меркаптиды алкилолова) более всего удобны для способов переработки ПВХ, требующих максимальной устойчивости к термическим ( в том числе и более 200 С) и механическим нагрузкам. [20]
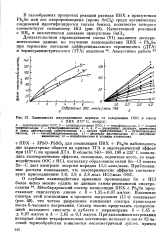 |
Зависимость индукционного периода от содержания ООС в смеси. [21] |
ООС; б - алкглярйпзгодныб GGG; 1 - тетрафеиилилиъи, 2 - хлорид трифснилолова; 3 -бутилтрифенилолово; 4, 5, в, 1 -дикаприлат, дилаурат, диметоксид и окись дибутилолова соответственно; - лаурат трибу тил олова; 9 - бутилстанновая кислота; 10 - гексабутилдистанноксан; 11 - дилаурат диоктилолова; 12 - дибутилди-винялолово; 13 - тетрабутилолово и хлориды алкилолова. [22]
Алкильные производные олова не разрушаются водой нри температуре до 100 С. Галогениды алкилолова и гидроокиси растворимы в воде; галегениды дают проводящие ток растворы, в которых они частично и обратимо гидролизо-ваны. [23]
Алкильные производные олова не разрушаются водой при температуре до 100 С. Галогениды алкилолова и гидроксиды растворимы в воде; галогениды дают проводящие ток растворы, в которых они частично и обратимо гидроли-зовакы. [24]
Тетраалкильные и тетраарильные производные олова не подвергаются действию воды при температуре 100 и только незначительно реагируют при гораздо более высоких температурах. Галогениды и гидроокиси алкилолова растворяются в воде [36]; при этом галоидопроизводные образуют сильно электропроводные растворы [37], в которых они частично и обратимо гидролизуются. Сильные основания сначала осаждают окиси диалкилолова, а затем снова их растворяют, образуя натриевые соли соответствующих кислот. Галоидопроизводные растворяются в спиртах без заметного соль-волиза; алкоксипроизводные можно получить действием на галоидопроизводные алгоколятов натрия. [25]
Реакции в большинстве случаев проходят в течение 3 час. Первый водородный атом тригидрида алкилолова реагирует быстрее, чем дигидриды диалкилолова, а последние быстрее, чем гидриды триалкилолова. Правда, этот тип реакций ограничен выбором олефинов, так как алюминийалкилы реагируют почти со всгми функциональными группами. [26]
В зависимости от условий реакции получают продукты с различным содержанием компонентов. Разделение смесей моно -, du -, трибромидов алкилолова осуществлялось на ряде неподвижных фаз: полиэтиленглико-ле 20 М, метилсиликоновом полимере SE-30, силиконовом полимере OF-1, фторированном силиконовом каучуке СКТФТ-50, нанесенных на различные носители: хромосорб - W, хромо-сорб - G и полихром-1. При исследовании было установлено, что лучшее разрешение, равное 2 4, достигнуто на полиэтилен-гликоле 20 М, нанесенном на фторопластовый. [27]
С помощью газовой хроматографии показано [8], что хлориды моно -, ди - и трибутилолова присутствуют в смеси даже при 200 С. Высказано предположение [8], что реакция между моно-и тригалогенидами алкилолова является обратимой. [28]
Большинство реакций соединений типа R4Sn состоит в замещении одной или нескольких органических групп. Важнейшими из этих реакций являются реакции расщепления соединений R4Sn до галогенидов алкилолова под действием галогенов, галогеноводо-родных кислот или галогенидов четырехвалентного олова. [29]
Сюда относятся неорганические каучуки, имеющие в полимерной цепи атомы фосфора и азота, а также оловянные каучуки на основе метакрилатов алкилолова, обладающие высокой химической стойкостью. [30]
Страницы: 1 2 3