Тепловое движение - молекула - растворитель
Cтраница 1
Тепловое движение молекул растворителя является причиной броуновского движения молекул растворенного вещества. Сущность его заключается в том, что о поверхность молекулы непрерывно ударяются молекулы жидкости - растворителя. При каждом ударе молекуле передается некоторый импульс. Удары происходят беспорядочно во времени и по направлению. Броуновское движение отражает тепловое движение молекул растворителя. [1]
При достаточно высокой температуре тепловое движение молекул растворителя преодолевает электростатические силы притяжения между растворителем и растворенным веществом и предотвращает сольватацию молекул. Так, например, Na2SO4 выше 32 4 С не образует кристаллогидрата. [2]
Эти силы могут преодолеваться тепловым движением молекул растворителя и звеньев цепей полимера уже при комнатных температурах. [3]
Эти силы могут преодолеваться тепловым движением молекул растворителя и звеньев цепей. [4]
Эти силы могут преодолеваться тепловым движением молекул растворителя и звеньев цепей полимера уже при комнатных температурах. [5]
Но простое строение двойного слоя нарушается тепловым движением молекул растворителя и ионов, а также взаимным отталкиванием одноименных ионов. В результате двойной слой приобретает размытое ( диффузное) строение. [7]
С повышением температуры, приводящим к росту теплового движения молекул растворителя, ДЛ рС увеличивается. [8]
Пока такого поля не было, ионы находились под влиянием теплового движения молекул растворителя и электростатического взаимодействия. Но когда внешнее поле между электродами возникло, на беспорядочное тепловое движение наложи-лось направленное перемещение ионов к электродам; так, например, катион будет двигаться к катоду. Но катион в растворе не вполне свободен. Он окружен ионной атмосферой, в которой преобладает заряд, противоположный по знаку центральному иону. [9]
Пока такого поля не было, ионы находились под влиянием теплового движения молекул растворителя и электростатического взаимодействия. Но когда внешнее поле между электродами возникло, на беспорядочное тепловое движение наложи-лось направленное перемещение ионов к электродам; так, например, катион будет двигаться к катоду. Но катион в растворе не вполне свободен. Он окружен ионной атмосферой, в которой преобладает заряд, противоположный по знаку центральному иону. [10]
Пока такого поля не было, ионы находились под влиянием теплового движения молекул растворителя и электростатического взаимодействия. Но когда внешнее поле между электродами возникло, на беспорядочное тепловое движение наложилось направ - ленное перемещение ионов к электродам; так, например, катион будет двигаться к катоду. Но катион в растворе не вполне свободен. Он окружен ионной атмосферой, в которой преобладает заряд, противоположный по знаку центральному иону. [11]
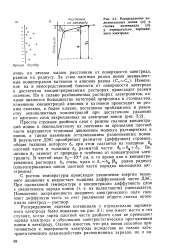 |
Распределение положительных ионов ( а и скачка потенциала ( б у отрицательно заряженного электрода. [12] |
Простое строение двойного слоя с резким скачком концентраций ионов к эквивалентному их значению за пределами плотной части нарушается тепловым движением молекул растворителя и ионов, а также взаимным отталкиванием разноименных ионов. В результате ДЭС приобретает размытое ( диффузное) строение, общая толщина которого 60 при этом слагается из толщины оф плотной части и толщины бд размытой части: 60 бЧ) - ( - бл. Величина бд зависит от природы и особенно от концентрации электролита. [13]
Как указывает Самойлов [32], для всестороннего рассмотрения вопроса о сольватации ионов в растворах электролитов нельзя ограничиваться определением чисел сольватации и энергии сольватации, а необходимо исследовать также и тс изменения, которые происходят при введении ионов не только в структуре растворителя, но п в характере теплового движения молекул растворителя. Все иышеуказанпые изменения в растворителе в основном обусловлены одной п той же причиной - - взаимодействием между попами п молекулами растворителя. [14]
Силы электростатического взаимодействия и силы теплового движения молекул растворителя способствуют переводу ионов из кристалла в раствор. При такой модели основным условием диссоциации является полярность растворителя. [15]
Страницы: 1 2 3
