Двуокись - плутоний
Cтраница 3
Окислы металлов IV группы, проявляющие устойчивую валентность 4, а именно окислы циркония и тория, а также двуокись плутония, имеющие кристаллическую структуру типа флюорита, образуют с двуокисью урана непрерывные ряды твердых растворов. [31]
Так как молекулы воды слабо связаны в этом соединении, то сильное нагревание приводит к потере ее с образованием двуокиси плутония. [32]
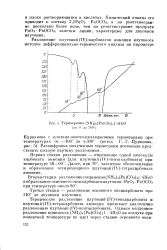 |
Термограмма ( ГШ4 б [ Ри ( СОз5 ] - лН20. [33] |
Химический анализ его приводит к составу 2 5РиС2 РиОСОз, а на рентгенограмме несколько более ясно, чем на рентгенограмме продукта РпОа РиОСОз, заметны линии, характерные для двуокиси плутония. [34]
Если в растворе е содержится примесей в больших, чем указано, количествах, то одно осаждение фениларсоната позволяет отделить примеси и количественно выделить плутоний, который может быть определен весовым путем - прокаливанием: фениларсоната плутония при 1100 С до двуокиси плутония. [35]
На основании анализа остающегося продукта и продуктов, выделившихся при прокаливании, можно сделать вывод, что в результате термического разложения кристаллического плутоний ( ГУ) - тетракарбоната натрия образуется так называемый скелетный кристалл, который состоит из сцементировавших-ся двух молекул соды и одной молекулы двуокиси плутония. [36]
Теплота образования PuOg равна - 246 5 ккал / моль. Двуокись плутония не восстанавливается водородом до металла. Попытки получить более высокие окислы плутония нагреванием РиО2 при 400 С и давлении кислорода 70 атм или прокаливанием ее при 800 С в атмосфере озона не дали положительных результатов. [37]
Двуокись плутония может быть переведена в РиРз нагреванием в токе смеси водорода и фтористого водорода при 400 - 600 СивРиР4 нагреванием при той же температуре в токе смеси кислорода и фтористого водорода или только в токе HF [ 3, стр. Под действием избытка графита двуокись плутония при 1200 - 1500 С переходит в карбид [ 3, стр. [38]
Подкладки из платины мало используются для работы вследствие трудности очистки ее от а-активности для повторного использования. Двуокись плутония удаляют с подкладки одним из описанных способов ( см. стр. [39]
Из окислов плутония в чистом виде получены закись ( моноокись) РиО и двуокись РиО2, наличие окиси трехвалентного плутония РиаО3 доказано лишь косвенными методами, а окись шестивалентного плутония отсутствует даже в виде смешанных окислов. Наиболее устойчива двуокись плутония - коричнево-желтоватый кристаллический порошок, получающийся при прокаливании солей четырехвалентного плутония, а также и солей других валентных состояний. [40]
Окислительно-восстановительное титрование Pu ( III) ванадатом аммония было применено П. Н. Палеем и Н. Е. Кочетковой ( 1955 г.) для определения содержания плутония в его двуокиси. В работе исследованы методы растворения двуокиси плутония, восстановление плутония до трехвалентного состояния на висмутовом редукторе, условия титрования, влияние примесей и возможность их отделения. [41]
Трийодид плутония получают при действии безводного йодистого водорода на металлический плутоний при температуре 450 С. При взаимодействии йодистого водорода с двуокисью плутония вместо трийодида образуется оксийодид плутония PuOJ. Все тригалогениды ( за исключением PuF3) легко растворяются в воде, свойства этих растворов обсуждаются ниже в разд. [42]
Двуокись плутония получают прокаливанием на воздухе любых соединений, за исключением фосфатов плутония. Драмонд и Уэлч [388] установили, чго состав двуокиси плутония в зависимости от исходного соединения может изменяться от РиО2 оо до Ри02 о9 за счет дополнительного поглощения кислорода. Прокаливание РиО2 на воздухе при 1200 С приводит к образованию окиси состава РиО2 0о2 - Более поздние исследования [189] подтвердили эти результаты. [43]
 |
Стальной кожух для защиты запаянной трубки. [44] |
Затем трубку нагревают при 300 - 325 С в течение 2 час. Этот метод удобен при растворении образцов, содержащих заметные количества двуокиси плутония. [45]
Страницы: 1 2 3 4