Чистая двуокись - углерод
Cтраница 3
Результаты, полученные для смесей углекислоты с водородом, интересно сопоставить с данными для чистой двуокиси углерода. Малые добавки водорода ( 3 %) приводят первоначально к исчезновению в продуктах реакции кислорода и озона. Однако при полном расходовании водорода и удалении его в виде конденсата в ловушке кислород и озон появляются вновь. При большом содержании водорода озон не обнаруживается. Малые добавки водорода ( до 10 %) также тормозят реакцию превращения двуокиси углерода - за одно и то же время степени превращения СО2 - общая и до СО - уменьшаются приблизительно в три раза. Но затем кривая Асо2 / ( % Н2) проходит через минимум и поднимается по закону, близкому к линейному. [31]
Результаты, полученные для смесей углекислоты с водородом, интересно сопоставить с данными для чистой двуокиси углерода. Малые добавки водорода ( 3 %) приводят первоначально к исчезновению в продуктах реакции кислорода и озона. Однако при полном расходовании водорода и удалении его в виде конденсата в ловушке кислород и озон появляются вновь. При большом содержании водорода озон не обнаруживается. Малые добавки водорода ( до 10 %) также тормозят реакцию превращения двуокиси углерода-за одно и то же время степени превращения С02 - общая и до СО - уменьшаются приблизительно в три раза. Но затем кривая Дсо2 / ( % Н2) проходит через минимум и поднимается по закону, близкому к линейному. [32]
Аналогично объясняется возникновение разрежения внутри куска при замене в окружающей среде инертного газа на чистую двуокись углерода. [33]
Соединения, содержащие только атомы углерода, водорода и кислорода, как правило, сгорают до чистой двуокиси углерода и воды. Наличие в соединении азота приводит к образованию небольших количеств азотной кислоты, растворяющейся в воде. Азотную кислоту можно легко определить аналитически и ввести соответствующую термохимическую поправку. [34]
При таких условиях обратимо абсорбируется приблизительно 0 25 моля двуокиси углерода на 1 моль хлорофилла в атмосфере чистой двуокиси углерода. Рабинович [53] наблюдал абсорбцию газообразной двуокиси углерода лишенным газов, сухим, кристаллическим зтилхлорофиллидом в вакууме. [35]
Кауко и Айрола [21, 31] предложили в качестве стандарта рН 0 0001 М раствор бикарбоната натрия, насыщенный чистой двуокисью углерода. Ионная сила этого буферного раствора так низка, что коэффициент активности может быть точно рассчитан по формуле Дебая и Хюккеля. Найдено, что ран этого стандартного раствора равен 4 038 при 0 С, 4 181 при 25 С и 4 237 при 38 С. [36]
Приготовленный раствор кипятят 20 мин в такой же кОлбе, как описано выше, н охлаждают в токе чистой двуокиси углерода. [37]
Приготовленный раствор кипятят 20 мин в такой же колбе, как описано выше, н охлаждают в токе чистой двуокиси углерода. [38]
 |
Установка для исследования диффузии в газах. [39] |
По указанным параметрам исследования видно, что измерения скорости диффузии производились недалеко от критической точки равновесия жидкость - пар чистой двуокиси углерода и ее смесей с азотом. Близость критической точки накладывает специфический отпечаток на процесс диффузии. Поэтому результаты исследования, которое не только-не является законченным, но находится лишь в первой половине своего пути, следует разбить на две части. [40]
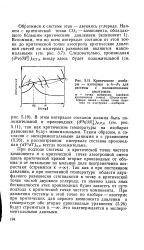 |
Критические изобары - изотермы в h - Nt для системы с положительным азеотропом. [41] |
Так как и при постоянном давлении, и при постоянной температуре области двухфазного равновесия стягиваются в точку в критической точке чистой двуокиси углерода, то именно здесь знак бесконечности этих производных будет зависеть от пути подхода к критической точке чистого компонента. [42]
Естественная концентрация бикарбонатных ионов в растворе возрастает в присутствии карбоната кальция, увеличиваясь в 500 раз в воздухе и в 140 раз в чистой двуокиси углерода. [43]
В круглодонной колбе с коротким горлом, снабженной резиновой пробкой с двумя трубками - длинной ( для подачи газа) н короткой ( отводной), кипятят воду н охлаждают ее в токе чистой двуокиси углерода. Когда вода охладится до 30 С, также под током двуокиси углерода вводят в колбу тонко измельченный ( порошкообразный) бикарбонат калия и растворяют его. Затем плотно закрывают колбу. [44]
Результаты опытов представлены также в виде коэффициента F ( табл. 2), равного отношению p / ps, где р - парциальное давление СО2 в воздухе при условиях опыта; ps - давление пара чистой двуокиси углерода над твердой фазой при той же температуре; величина р получена как произведение давления воздуха на молярную концентрацию двуокиси углерода, соответствующую состоянию насыщения. [45]
Страницы: 1 2 3 4