Гидратированная двуокись
Cтраница 1
Гидратированная двуокись представляет собой темно-зеленый осадок; образуется при кипячении нейтрального раствора NaaRhCle с броматом натрия. [1]
Гидратированная двуокись выделяется в виде темно-синего осадка при действии едкой щелочи или бикарбоната на кипящий раствор 1 га31гС16, а также путем броматного гидролиза. [2]
Гидратированные двуокиси палладия, родия, иридия, осмия и рутения нерастворимы и используются в анализе для определения перечисленных элементов. Окись двухвалентного палладия и окислы платины не имеют аналитического применения; гидратированная двуокись палладия осаждается броматнкм гидролизом и, подобно двуокиси марганца, кипячением азотнокислого раствора с броматом натрия и азотнокислой ртутью. [3]
Гидратированная двуокись олова, так называемая оловянная кислота, существует в виде двух форм, различающихся по химической активности. [4]
Гидратированная двуокись свинца РЬО2 - лН2О получается при гидролизе плюмбатов и окислении солей свинца в водных растворах. Гидрата определенного состава, по-видимому, не существует. [5]
Гидратированная двуокись титана представляет собой мелкокристаллическую или аморфную фазу. [6]
Гидратированную двуокись германия фильтруют, промывают очищенной водой, спиртом и сушат при 150 - 200 С. При этой температуре GeO2 полностью обезвоживается. Сушку ведут в противнях из кварца в электрических муфельных печах. [7]
Гидратированную двуокись олова удается получить, нагревая металлическое олово с конц. [8]
Образовавшуюся гидратированную двуокись марганца отфильтровывают и определяют при помощи стандартного раствора гидрохинона прямым или непрямым методом. [9]
Гидролитическое получение гидратированной двуокиси германия осуществляется смешением с водой галогенида или раствора его в органическом растворителе. Равновесие гидролитической реакции достигается довольно медленно, и процесс заканчивается только после продолжительного перемешивания. Аппаратуру изготовляют из кварца, полиэтилена или пластмасс особых марок. Двуокись германия отфильтровывают, промывают водой, спиртом, сушат и прокаливают. [10]
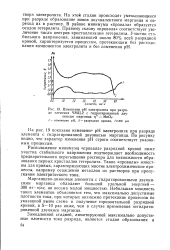 |
Изменение рН электролита при разряде элемента ЧМЦ-2 с гидратированной двуокисью марганца т - МпСЬ. / - изменение рН, 2 - разрядная кривая, / 300 ца. [11] |
Марганцево-цинковые элементы с гидратированными двуокисями марганца обладают большой удельной энергией - 300 вт ч / кг, но весьма малой мощностью. Небольшая мощность таких элементов объясняется тем, что максимально допустимые плотности тока, при которых возможно протекание процессов по указанной выше схеме и получение горизонтальной разрядной кривой, в 5 - 10 раз ниже, чем в случае применения негидрати-роваиной двуокиси марганца. [12]
Образующаяся в процессе окисления гидратированная двуокись марганца сорбирует гидроокись таллия, что содействует более полному ее осаждению. [13]
Для облегчения фильтрации осадка гидратированной двуокиси через суспензию перед фильтрацией пропускают в течение 30 мин углекислый газ. Для извлечения оставшегося в фильтрате рения окисляют низшие его соединения перекисью водорода до HReO4, нейтрализуют раствор аммиаком и выделяют перренат аммония, возвращаемый в цикл восстановления. Двуокись рения восстанавливают водородом в молибденовых лодочках ( высота насыпки - 20 мм) вначале при 400, затем при 600 С с выдержкой в течение 1 ч при каждой температуре. [14]
Высокопористых соединений на основе гидратированной двуокиси олова подобным методом ранее получено не было. Необходимым условием их синтеза сорбционным путем является использование окисных модификаций исходных продуктов, обладающих пористой каркасной структурой. Известные способы синтеза активной двуокиси олова [3-5] приводят к получению высокодисперсных порошков, поэтому задачей данного исследования были и разработка способа получения высокопористого образца активной двуокиси олова, и выяснение возможности ее превращения в новые высокопористые соединения, что было сделано на примере взаимодействия двуокиси олова с ионами меди, которые, как было показано ранее I3 8 ], сорбируются двуокисью олова в значительных количествах. [15]
Страницы: 1 2 3 4