Гидратированная двуокись
Cтраница 3
При окислении двухвалентного марганца мы нашли, что один из трех кислородов гидратированной двуокиси марганца быстро обменивается с водой уже при промывании осадка. Обмен более чем одного атома не был найден даже при кипячении осадка с водой на протяжении нескольких часов. [31]
Раствор разбавляют большим количеством холодной воды; выпавший при этом белый осадок гидратированной двуокиси олова после нагревания несколько раз промывают декантацией, отфильтровывают и снова промывают на фильтре с отсосом. Затем полученный продукт высушивают, прокаливают в фарфоровом тигле при 700 - 800 С. [32]
В широком интервале температур и концентраций наиболее устойчивыми соединениями германия и кремния являются гидратированные двуокиси этих элементов. [33]
Соли Мп ( IV) в водном растворе почти полностью гидролизуются с образованием гидратированной двуокиси марганца. [34]
При кипячении с броматом натрия и нейтрализации раствора содой образуется синевато-черный осадок, гидратированной двуокиси иридия; промытый осадок вновь растворяют при нагревании в соляной кислоте, причем образуется темно-синий раствор, который становится после продолжительного кипячения сначала зеленым, а затем бурым. [35]
Как коллектор для концентрирования металлов, образующих легко гидролизующиеся соли, хорошо зарекомендовала себя гидратированная двуокись марганца. В качестве коллекторов в химическом анализе природных и сточных вод используют фосфаты металлов. [36]
В результате этих реакций образуется взвесь хлопьевидных частиц фтористого кальция, кальциевых солей фосфорной кислоты и гидратированной двуокиси кремния, и ранее осветленная вода вновь превращается в суспензию. Развитая поверхность полученных хлопьевидных частиц должна обеспечить практически полное соосаждение высокодисперсной фосфорсодержащей взвеси, не удаленной из сточной воды при первичном осветлении. [37]
С нитратом двухвалентной ртути раствор стано вится желтым, при кипячении с броматом натрия выделяется бурый осадок гидратированной двуокиси. [38]
Было показано [37], что из растворов солей рениевой кислоты при действии цинка и соляной кислоты количественно осаждается гидратированная двуокись рения Re02 2Н20; эта реакция была использована для определения элемента. Другие исследователи [38] позже утверждали, что полученное таким образом вещество может быть не вполне чистым и что оно не всегда соответствует вышеприведенной формуле. [39]
Содержание О18 меньше на 1 / 3, чем в исходной воде, объясняется быстрым обменом одного кислородного атома гидратированной двуокиси марганца с водой во время промывания осадка. Обмен большего числа атомов не был найден даже при кипячении осадка с водой на протяжении нескольких часов. Если гидрати-рованную двуокись марганца, которую правильней изображать формулой Мп02 Н2О, полученную в опыте с меченой водой, промыть не обычной, а тяжелокислородной водой, то ее изотопный состав ( 0 91 %) практически не отличается от изотопного состава исходной воды. [40]
К раствору, который должен содержать Na2C03, прибавляют избыточное количество соли марганца ( II), при этом образуется гидратированная двуокись марганца, а IOj-ионы восстанавливаются до Юз-ионов. [41]
К раствору, который должен содержать Na2G03, прибавляют избыточное количество соли марганца ( II), при этом образуется гидратированная двуокись марганца, а IOj-ионы восстанавливаются до Юз-ионов. [42]
Другой метод - обработка водного экстракта из продукта окислительного сплаапения - состоит в добавлении спирта для осаждения рутения в ннде гидратированной двуокиси. Последнюю отделяют путем фильтрования, а осмий выделяют из фильтрата осаждением в виде осмата калия при добавлении избыточного количества едкого кали. [43]
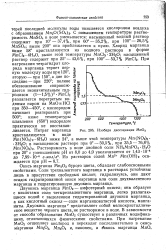 |
Изобара диссоциации МпО2. [44] |
Двуокись марганца МпО2 - амфотерный окисел; она образует с кислотами соли четырехвалентного марганца, легко разлагающиеся водой с выделением гидратированной двуокиси марганца, а как кислотный окисел - соли марганцоватистой кислоты, манга-йиты. Двуокись марганца7 представляет собой мелкокристаллическое вещество черного цвета, не растворимое в воде. В зависимости от способа образования МпО2 существует в различных модификациях, отличающихся физическими свойствами. [45]
Страницы: 1 2 3 4