Образующаяся двуокись - азот
Cтраница 1
Образующаяся двуокись азота NO2 частично растворяется в еще не разложившейся кислоте, окрашивая ее в желтый или красно-бурый цвет, а частично выделяется в виде дыма. Этим обусловлено название такой кислоты - дымящая. [1]
Образующаяся двуокись азота окрашивает кислоту в желтый цвет. [2]
 |
Сорта азотной кислоты и их некоторые физические константы. [3] |
Образующаяся двуокись азота остается в растворе и сообщает ему желтую окраску. [4]
Образующаяся двуокись азота NO2 растворяется в еще не разложившейся кислоте, окрашивая ее в желтый или красно-бурый цвет, а частично выделяется в виде дыма. Этим обусловлено название такой кислоты - дымящая. [5]
Образующаяся двуокись азота растворяется, и вода постепенно поднимается вверх. Если окись азота и кислород не содержат воздуха, то почти весь цилиндр заполняется водой. [6]
Образующаяся двуокись азота растворяется в HNO3, окрашивая ее в красно-бурый цвет. Такую кислоту называют дымящей азотной кислотой. [7]
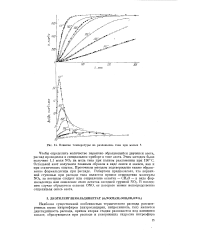 |
Влияние температуры на разложение тэна при малых Л. [8] |
Чтобы определить количество первично образующейся двуокиси азота, распад проводился в специальном приборе в токе азота. Этим методом было получено 1 1 моля N02 на моль тэна при полном разложении при 190 С. [9]
Опыт лучше вести в дневное время, так как образующаяся двуокись азота при искусственном освещении плохо видна. [10]
Однако ни-трозные газы, выходящие из конденсаторов 7 и 8, можно полностью окислить до МСЬ, а затем поглотить образующуюся двуокись азота концентрированной азотной кислотой при охлаждении. При нагревании нитрозные газы выделяются из раствора и перерабатываются в автоклаве в 98 % - ную кислоту. В этом случае в концентрированную кислоту можно перевести до 70 % окислов азота и лишь 30 % выделить из скоростного холодильника 5 в виде разбавленной 30 % - ной кислоты. Такое варьирование придает гибкость предлагаемой схеме и позволяет изменять количества выпускаемых концентрированной и разбавленной кислот в зависимости от требований потребителей. [11]
Современное производство азотной кислоты из аммиака включает следующие основные стадии: очистка аммиака и воздуха, контактное окисление аммиака до окиси азота, охлаждение нитрозных газов, окисление окиси азота и поглощение образующейся двуокиси азота водой. Выделяющаяся при этом окись азота возвращается в процесс и снова подвергается окислению. [12]
 |
Поглотитель для двуокиси азота.| Промывная склянка. [13] |
Очищенный от примесей газ поступает для окисления в склянку 7 с кислым раствором перманганата калия и затем в последовательно соединенные поглотители 8, содержащие смесь растворов сульфаниловой кислоты и я-нафтиламина или раствор метафенилендиамина для поглощения образующейся двуокиси азота. Ловушки 9 служат для предохранения от перебрасывания растворов. [14]
Преимущество процесса заключается в том, что при отсутствии водяных паров в газах силикагель можно применять как в качестве катализатора процесса окисления NO в МО2 без предварительного удаления воды из газов, так и в качестве адсорбента образующейся двуокиси азота. [15]
Страницы: 1 2