Трассерная диффузия
Cтраница 1
Трассерная диффузия зависит также от вязкости жидкости. По Милзу и Кеннеди [153], произведение D t для ионов К и Rb зависит линейно от УС. Как установлено авторами, трассерная диффузия этих и других негидратированных ионов определяется главным образом двумя факторами. С одной стороны, молекулы растворителя должны уйти с траектории движения диффундирующего иона. [1]
Трассерная диффузия этих двух ионов одинаково зависит от природы фонового электролита. [2]
Трассерная диффузия ионов отличается от обычной диффузии и в отношении других проявлений электрических сил между ионами. Электрофоретический эффект, зависящий от концентрации, становится пренебрежимо малым, так как концентрация диффундирующего меченого иона очень низка. Эффект релаксации сохраняет свое значение, так как меченый ион диффундирует в относительно неподвижной среде, что проявляется в деформации ионной сферы и уменьшении подвижности. В обычной диффузии бинарных электролитов каждый вид ионов диффундирует с одинаковой скоростью, так что ионная сфера сохраняется сферически симметричной. [3]
Трассерная диффузия ионов водорода особенно интересна. Это можно объяснить тем, что ион водорода движется не только за счет гидродинамического перемещения иона оксония ( Н3О), но также и благодаря прототропному механизму ( см. разд. Это, вероятно, объясняется - тем, что ион К, обладающий близким к молекуле Н2О размером, почти не деформирует структуру воды. Однако имеющий малый размер ион Li с высокой плотностью поверхностного заряда оказывает сильное разрушающее влияние на структуру воды даже при такой низкой концентрации, при которой влияние ионов К пренебрежимо мало. Ориентированное положение молекул воды в гидратной оболочке иона Li отличается от структуры молекул воды, связанных только водородными связями, и это затрудняет перенос протона между молекулами воды. [4]
Коэффициент трассерной диффузии можно определить независимо для разных сортов ионов. В отличие от обычной диффузии ограничение, связанное с тем, что ионы с зарядом противоположного знака должны диффундировать с одинаковой скоростью, в этом случае не имеет силы. Из-за высокой концентрации фонового электролита, присутствующего в постоянной концентрации, диффундирующий меченый ион не вызывает появления заметного диффузионного потенциала, следовательно, скорость его диффузии практически не изменяется под действием эффекта наложения электрического поля. [5]
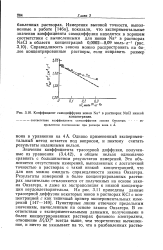 |
Коэффициент самодиффузии ионов Na в растворах NaCl низкой. [6] |
Значения коэффициента трассерной диффузии, полученные из уравнения (3.4.42), в общем нельзя однозначно сравнить с большинством результатов измерений. Это объясняется отсутствием измерений, выполненных с достаточной точностью в растворах с такой низкой концентрацией, что для них можно ожидать справедливости закона Онзагера. Результаты измерений в более концентрированных растворах значительно отклоняются от полученных на основе закона Онзагера, и даже их экстраполяция к низкой концентрации неудовлетворительна. Пунктирные линии отвечают предельным значениям, вычисленным на основе закона Онзагера. [7]
В условиях трассерной диффузии общая концентрация и ионная сила электролита почти одинаковы во всем объеме раствора. Таким образом, его коэффициент активности также везде одинаков и градиент химического потенциала диффундирующего меченого иона можно с удовлетворительной точностью выразить через градиент концентрации даже в достаточно концентрированных растворах. При этом термодинамический фактор не входит в выражение для коэффициента диффузии. [8]
Так как ионы при трассерной диффузии и самодиффузии перемещаются независимо один от другого, их движение не зависит от скорости, с которой переносятся ионы противоположного знака. [9]
К в растворе КС1), трассерная диффузия становится идентична самодиффузии. [10]
Эти последние два уравнения - предельный закон Онзагера для трассерной диффузии и самодиффузии; можно предположить, что он справедлив только для растворов с низкой ионной силой из-за упрощающих предположений, использованных при его выводе и не рассмотренных детально в данной главе. [11]
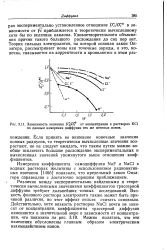 |
Зависимость значения D i / Df от концентрации в растворах КС1 по данным измерения диффузии тех же меченых ионов. [12] |
Различия между экспериментально найденными и теоретически вычисленными значениями коэффициентов трассерной диффузии требуют дальнейших точных исследований. Вязкость фонового раствора электролита также может быть причиной различия, но этот эффект нельзя считать основным. Действительно, хотя вязкость растворов NaCl почти не зависит от концентрации, коэффициенты трассерной диффузии изменяются в значительной мере в зависимости от концентрации, что показано на рис. 3.10. Можно полагать, что эти изменения обусловлены главным образом электрическим взаимодействием ионов. [13]
Диффузия меченных изотопами молекул в действительности представляет собой предельный случай трассерной диффузии в однородной жидкости. Трассерная диффузия представляет собой диффузию одного компонента, присутствующего в очень низкой концентрации в растворе с одинаковым во всей системе составом. Другими словами, компонент, присутствующий в растворе в виде следов, имеет отличный от нуля градиент концентрации, в то время как градиент концентрации других компонентов, имеющих по сравнению с первым высокую концентрацию, равен нулю. Трассерная диффузия имеет место, например, когда ионы Na, присутствующие в пренебрежимо низкой концентрации, диффундируют в растворе КС1, имеющем постоянную концентрацию. [14]
В связи со сравнением экспериментальных и теоретических данных следует отметить, что экспериментальная техника измерения трассерной диффузии очень чувствительна и данные измерений в представляющихся одинаковыми условиях, но разными методами часто заметно различаются - - иногда даже по их характеру. Так, Уонг и Миллер [150] нашли, что кривая зависимости коэффициента самодиффузии ионов Na, построенная как функция корня квадратного из ионной силы раствора NaCl, проходит через максимум, в то время как в исследованиях [151] и [152] этого не наблюдалось. [15]
Страницы: 1 2