Дегидрохлорирование - поливинилхлорид
Cтраница 2
 |
Дегидрохлорирование сополимера винилхло-рида ( 60 % и винилиденхлорида ( 40 % при различной скорости пропускания воздуха. [16] |
Таким образом, вопрос об автокаталитическом действии хлористого водорода при дегидрохлорировании поливинилхлорида даже в условиях окисления не является окончательно решенным. [17]
Как видно из рис. 1, относительная скорость поглощения кислорода резко снижается при переходе от поливи-нилена, полученного эквимолярным дегидрохлорированием поливинилхлорида, к поливинилснхлориду, полученному на основе поли-винилиденхлорида. Поливиниленхлорид устойчив к кислороду при комнатной температуре. [18]
Как видно из рис. I, относительная скорость поглощения кислорода резко снижается при переходе от поливи-нилена, полученного эквимолярным дегидрохлорированием поливинилхлорида, к поливиниленхлориду, полученному на основе поли-винилиденхлорида. Поливиниленхлорид устойчив к кислороду при комнатной температуре. [19]
Отмеченное выше наличие ненасыщенных концевых групп и повышение подвижности хлора в аллильных звеньях может влиять на инициирование и дальнейшее развитие процесса дегидрохлорирования поливинилхлорида по свободнорадикально-му механизму. [20]
Если при разложении поливинилхлорида в результате термоокислительного процесса образуются перекисные соединения, то при одновременном отщеплении хлористого водорода может развиваться цепной радикальный процесс дегидрохлорирования поливинилхлорида. С другой стороны, перекиси инициируют присоединение хлористого водорода к олефинам. Соответствующая аналогия может, очевидно, быть распространена и на по-ливинилхлорид при 140 - 190 С. [21]
Если при дегидрохлорировании низкомолекулярных модельных соединений на начальной стадии в реакцию вступают молекулы такого же строения, как и в конце процесса, то при дегидрохлорировании поливинилхлорида в каждый момент реакции хлористый водород отщепляется от макромолекул различной структуры. Воспользоваться для расчета методом стационарных концентраций, предполагающим неизменное содержание промежуточных продуктов, из-за особенностей распада полимера не представлялось целесообразным и поэтому было выведено дифференциальное уравнение, характеризующее реакцию дегидрохлорирования. При выводе уравнения использована теория абсолютных скоростей химических реакций Вина - Джонса и Эйрин-га, учитывающая при определении кинетических параметров термодинамические факторы. Было принято также допущение о том, что дегидрохлорирование является мономолекулярным стохастическим процессом. Это допущение не противоречит известному положению о том, что при влиянии на какой-либо процесс многих факторов, из которых ни один не является существенно преобладающим, вероятность события определяется нормальной функцией распределения. Можно допустить, что скорость отщепления хлористого водорода от лабильных групп различной химической природы, находящихся в сегментах цепей с различной тактичностью, в целом описывается нормальной функцией распределения. [22]
Термическое дегидрохлорирование насыщенных полимеров является автокаталитическим процессом, поэтому скорость реакции повышается по мере накопления продуктов деструкции. Дегидрохлорирование поливинилхлорида ускоряется также введением в полимер галогенидов алюминия и железа. В присутствии стеара-тов этих металлов быстрое образование окрашенных продуктов происходит при облучении полимера ультрафиолетовым светом или действии частиц высоких энергий. Однако задача получения полисопряженных систем с целью создания полупроводниковых материалов была поставлена лишь в последние годы. Этот исследователь провел дегидрохлорирование поливинилиденхлорида, используя в качестве дегидрохлорирующих реагентов органические основания ( морфолин) или спиртовый раствор щелочи. [23]
Температура стеклования поливинилхлорида составляет 78 - 105 С, температура хрупкости около 80 С, температура текучести порядка 200 С. При температуре выше 100 С начинается дегидрохлорирование поливинилхлорида с изменением окраски от желтоватой до черной. Для повышения стойкости поливинилхлорида в него вводят стабилизаторы. [24]
Температура стеклования поливинилхлорида составляет 78 - 105 С, температура хрупкости около 80 С, температура текучести порядка 200 С. При температуре выше 100 С начинается дегидрохлорирование поливинилхлорида с изменением окраски от желтоватой до черной. Сшивание макромолекул полимера начинается при 175 С, а также при ультрафиолетовом облучении. Для повышения стойкости поливинилхлорида в него вводят стабилизаторы. [25]
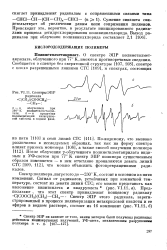 |
Спектры ЭПР. [26] |
Сужение синглета свидетельствует об увеличении длины цепи сопряжения полиенов. Происходит это, вероятно, в результате инициированного радикалами процесса дегидрохлорирования поливинилхлорида. [27]
 |
Зависимость температуры стеклования Гд пленки ПИЛ от количества пластификатора q.| Хроматограмма спиртовых экстрактов образцов пленок ПИЛ. [28] |
В образцах пленок, испытывавшихся при температуре 363 К, на хрома-тограмме ( рис. 5) над пятнами диоктилфталата обнаружено вещество, которое не наблюдалось в пленках, испытывавшихся при более низких температурах. Можно предположить, что это вещество является продуктом гидролиза отдельных низкомолекулярных составляющих изоляционного материала под действием раствора соляной кислоты, образующейся вследствие дегидрохлорирования поливинилхлорида при наличии грунтовой влаги, или продуктом омыления диоктилфталата. [29]
 |
Гидрирование поли-винилена ( / и поливиниленхло-рида ( 2 в декалине при 100 С и давлении водорода 200 am ( катализатор N1 Ренея. [30] |
Страницы: 1 2 3